题目内容
8.用化学方法除去下列物质中的少量杂质(括号中为杂质),写出有关反应方程式(1)Cu(Zn)Fe+2HCl=FeCl2+H2↑(合理即可).
(2)CO2(CO)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)CO(CO2)CO2+2NaOH═Na2CO3+H2O.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)根据金属活动性顺序,铁能和酸反应,铜和酸不反应,故可用盐酸(或稀硫酸)除去铁,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑(合理即可).
(2)根据一氧化碳和二氧化碳的化学性质,一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,二氧化碳不与氧化铜不反应,故可将混合气体通过灼热的氧化铜,反应的化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)据一氧化碳和二氧化碳的化学性质,二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,一氧化碳不与氢氧化钠溶液反应,故可将混合气体通入氢氧化钠溶液中,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
故答案为:(1)Fe+2HCl=FeCl2+H2↑(合理即可);(2)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;(3)CO2+2NaOH═Na2CO3+H2O.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.自然界中最坚硬的物质是( )
| A. | 金刚石 | B. | 铁丝 | C. | 铝丝 | D. | 铜丝 |
3.饲养金鱼的人每天都需要用新鲜水换掉鱼缸中的旧水,但如果在缸内放置一些金鱼藻,则可延长换水时间,其主要原因是( )
| A. | 金鱼以金鱼藻为食 | |
| B. | 金鱼藻可制造葡萄糖供金鱼食用 | |
| C. | 金鱼藻可吸附水中污物,保持水清洁 | |
| D. | 金鱼藻可吸收金鱼排出的CO2,并释放氧气供金鱼需要 |
13.下表是农作物秸杆和煤含硫等相关数据,通过分析表数据回答下列问题:
(1)若选择秸杆为发电燃料,其优点有:燃烧秸秆能减少空气污染物二氧化硫的排放,减少酸雨产生;秸秆是可再生能源
(2)你对电厂发电的其他建议可以选用含硫更少的燃料作为发电厂的燃料;选用天然气为发电厂的燃料;选用太阳能发电.
| 秸杆 | 煤 | |
| 平均含硫量 | 0.38% | 1% |
| 电厂发电消耗量,年 | 2.0x105t | 1.0xlO5t |
| 产生二氧化硫,年 | 1520t | 2000t |
(2)你对电厂发电的其他建议可以选用含硫更少的燃料作为发电厂的燃料;选用天然气为发电厂的燃料;选用太阳能发电.
18.写出下列反应的化学方程式,并简答.
| 化学反应 | 化学方程式 | 简答 |
| 煅烧石灰石 | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | 反应类型为分解反应 |
| 铁丝在氧气中燃烧 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | 生成物颜色为黑色 |
| 碳和氧化铜在高温下反应 | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | 该反应中氧化剂为氧化铜 |
| 二氧化碳通入足量的澄清石灰水 | CO2+Ca(OH)2═CaCO3↓+H2O | 此反应可鉴定二氧化碳 |
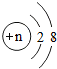 中,若n为不同数值可表示核外电子排布相同的不同微粒.
中,若n为不同数值可表示核外电子排布相同的不同微粒.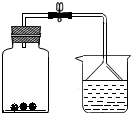 如图所示,向盛有红棕色二氧化氮(NO2)气体的集气瓶中投入几小块木炭或活性炭,最终观察到集气瓶内红棕色消失(填“变深”、“不变”或“消失”),漏斗中液面上升(填“上升”、“下降”或“不变”).其原因是:活性炭有吸附 作用,使瓶中气体压强小于外界大气压(填“大于”、“等于”或“小于”).根据木炭或活性炭的这一性质,写出其在生产、生活中的一种用途制糖工业中作脱色剂(或防毒面具里作滤毒剂等).
如图所示,向盛有红棕色二氧化氮(NO2)气体的集气瓶中投入几小块木炭或活性炭,最终观察到集气瓶内红棕色消失(填“变深”、“不变”或“消失”),漏斗中液面上升(填“上升”、“下降”或“不变”).其原因是:活性炭有吸附 作用,使瓶中气体压强小于外界大气压(填“大于”、“等于”或“小于”).根据木炭或活性炭的这一性质,写出其在生产、生活中的一种用途制糖工业中作脱色剂(或防毒面具里作滤毒剂等).