题目内容
18.将表面生锈的铁钉放入盛有足量稀盐酸的试管中,现象是:铁锈消失,无色液体逐渐变成黄色,写出化学方程式:Fe2O3+6HCl═2FeCl3+3H2O;过一段时间以后看到铁钉表面有气泡产生,写出化学方程式:Fe+2HCl═FeCl2+H2↑.分析 铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁与水,铁锈完全消失后,铁与稀盐酸反应生成氯化亚铁和氢气,据此写出反应的化学方程式即可.
解答 解:铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应现象为:铁锈逐渐溶解,溶液由无色变成黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
当铁锈完全反应后,铁与盐酸发生反应,生成氯化亚铁与氢气,会观察到有气泡产生,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:黄色;Fe2O3+6HCl═2FeCl3+3H2O;有气泡产生;Fe+2HCl═FeCl2+H2↑.
点评 本题难度不大,主要考查酸的化学性质,掌握铁锈的主要成分、酸的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
1.下列变化不属于缓慢氧化的是( )
| A. | 铁生锈 | B. | 酒精燃烧 | C. | 塑料老化 | D. | 人的呼吸 |
13.下列各组物质在给定条件下能大量共存的是( )
| A. | 在PH=1的溶液中:KCl、Na2SO4 HNO3 | |
| B. | 在PH=2的溶液中:NaCl、Na2CO3、Na2SO4 | |
| C. | 在PH=13的溶液中:BaCl2、Na2CO3、NaOH | |
| D. | 在PH=14的溶液中:FeCl3、Ba(NO3)2、CaCl2 |

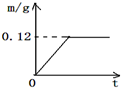 小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器. (相关化学方程式:H2SO4+Zn═ZnSO4+H2↑)
小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器. (相关化学方程式:H2SO4+Zn═ZnSO4+H2↑)