题目内容
(2013?徐汇区二模)“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).
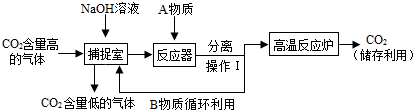
请根据“捕捉”CO2过程图回答问题:
①加入A物质的化学式是
②可循环利用的B物质中一定含有的物质是
③该过程中还可循环利用的物质是

请根据“捕捉”CO2过程图回答问题:
①加入A物质的化学式是
Ca(OH)2
Ca(OH)2
;分离操作Ⅰ的名称是过滤
过滤
;写出高温反应炉中发生反应的化学方程式CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;
| ||
②可循环利用的B物质中一定含有的物质是
NaOH
NaOH
,可能含有的物质是Na2CO3或Ca(OH)2
Na2CO3或Ca(OH)2
.③该过程中还可循环利用的物质是
CaO
CaO
.分析:①根据生石灰与水结合生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀考虑,根据液体与不溶于液体的固体分离方法和方程式的书写考虑;②根据碳酸钠与氢氧化钙反应的生成物考虑;③根据循环利用的物质是指在前面的反应中是反应物,后面的反应中是生成物.
解答:解:①在捕捉室中氢氧化钠与二氧化碳反应生成碳酸钠,进入反应器,所以加入的A物质与碳酸钠反应生成难溶物,高温能放出二氧化碳,所以A物质可以是氧化钙或氢氧化钙;固体和液体分离的方法是过滤,碳酸钙高温生成氧化钙和二氧化碳,反应条件是高温,二氧化碳后面标上上升符号;
②碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;如果碳酸钠与氢氧化钙反应时,碳酸钠过量,还可能含有碳酸钠,如果氢氧化钙过量,就含有氢氧化钙;
③由于最后碳酸钙高温生成氧化钙和二氧化碳,前面加入的A可以是氧化钙,所以氧化钙还可循环利用.
故答案为:①Ca(OH)2;过滤;CaCO3
CaO+CO2↑;②NaOH;Na2CO3或Ca(OH)2; ③CaO.
②碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;如果碳酸钠与氢氧化钙反应时,碳酸钠过量,还可能含有碳酸钠,如果氢氧化钙过量,就含有氢氧化钙;
③由于最后碳酸钙高温生成氧化钙和二氧化碳,前面加入的A可以是氧化钙,所以氧化钙还可循环利用.
故答案为:①Ca(OH)2;过滤;CaCO3
| ||
点评:解答本题关键是要知道循环利用的物质是指在前面的反应中是反应物,后面的反应中是生成物,还要熟悉方程式的书写.

练习册系列答案
相关题目
 )和乙(
)和乙( )两种不同的分子,它们在一定条件下能发生化学反应,反应前后的微观变化如图所示,下列说法正确的是( )
)两种不同的分子,它们在一定条件下能发生化学反应,反应前后的微观变化如图所示,下列说法正确的是( )
 (2013?徐汇区二模)固体物质R在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示.下列说法正确的是( )
(2013?徐汇区二模)固体物质R在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示.下列说法正确的是( )