题目内容
6.甲、乙两位同学在学完酸的化学性质后,做了如下实验:
写出甲实验中盐酸和氢氧化钙反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
乙实验中盐酸和碳酸钠反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑.
实验结束后,甲、乙两位同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论.
【观察与讨论1】
甲同学在做实验时没有观察到明显现象,于是对氢氧化钙溶液和稀盐酸能发生反应表示怀疑.但乙同学认为,甲同学实验时应先向氢氧化钙溶液中滴几滴酚酞溶液,再滴加适量的稀盐酸,当观察到酚酞溶液由红色变无色时,就可以说明两种物质能发生反应.
【观察与讨论2】当乙同学沿废液缸内壁缓慢倾倒液体时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀.经过讨论确定,甲、乙同学实验后的试管内废液中含有的溶质分别是CaCl2、HCl,NaCl、Na2CO3(均写化学式),才会出现上述现象.
分析 根据反应物和生成物按照反应规律书写出相应的化学方程式;
【观察与讨论1】向氢氧化钙溶液中应先滴几滴酚酞试液,则溶液为红色,如果红色消失,则说明反应;
【观察与讨论2】废液缸中先有气泡产生,然后又出现了白色沉淀,说明液体中有酸和碳酸根及钙离子;所以知甲同学的试管含有CaCl2、HCl;乙同学的试管中含有NaCl、Na2CO3
解答 解:盐酸和氢氧化钙反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O
盐酸和碳酸钠反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑
【观察与讨论1】酚酞溶液遇碱性溶液会变红;而在中性或酸性溶液中显示无色;酚酞溶液可鉴别碱是否被中和;
【观察与讨论2】废液缸中先有气泡产生,然后又出现了白色沉淀,通过反应可知:①盐酸和氢氧化钙溶液生成氯化钙和水,②盐酸和碳酸钠生成氯化钠和水和二氧化碳;另外还应考虑盐酸和碳酸钠过量;所以知甲同学的试管含有CaCl2、HCl;乙同学的试管中含有NaCl、Na2CO3;
故答案为:Ca(OH)2+2HCl═CaCl2+2H2O
Na2CO3+2HCl═2NaCl+H2O+CO2↑
【观察与讨论1】酚酞溶液由红色变无色(或酚酞溶液红色褪去)
【观察与讨论2】CaCl2、HCl; NaCl、Na2CO3
点评 本题主要考查化学实验方案的设计与评价,根据物质的性质和物质间的反应规律,学会运用猜想与事实验证的方法和技巧处理实验问题.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
16.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,正确的是( )
| A. | 茶氨酸属于有机高分子化合物 | |
| B. | 茶氨酸中碳元素与氢元素的质量比为1:2 | |
| C. | 茶氨酸中碳元素的质量分数最大 | |
| D. | 一个茶氨酸分子中含有一个氮分子和一个臭氧分子 |
1.将60g镁、铁、铝的混合物放入到一定质量的稀硫酸中恰好完全反应,收集到氢气4g,将反应后的溶液蒸干可得硫酸盐的质量是( )
| A. | 202g | B. | 256g | C. | 252g | D. | 不能确定 |
15.下列叙述中,不符合质量守恒定律的是( )
| A. | 蜡烛燃烧后的余烬所剩无尽 | |
| B. | 取20克石灰石于烧杯中再向其中加入50克稀盐酸恰好完全反应,反应后烧杯中物质总质量为66.7克 | |
| C. | 4g食盐晶体溶于96g水中,溶液的质量为100g | |
| D. | 10g镁带在空气中燃烧后,生成物的质量为18g比镁带质量增加了 |
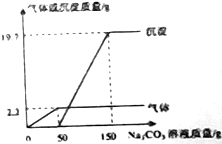 在实验课上,同学们用Ba(OH)2和稀盐酸做中和反应的实验探究,小亮取反应后的溶液105.9g,滴入碳酸钠溶液,先后有气体和白色沉淀生成.加入碳酸溶液与生成沉淀的气体的质量关系如图所示.
在实验课上,同学们用Ba(OH)2和稀盐酸做中和反应的实验探究,小亮取反应后的溶液105.9g,滴入碳酸钠溶液,先后有气体和白色沉淀生成.加入碳酸溶液与生成沉淀的气体的质量关系如图所示.