题目内容
17.实验室进行过滤和蒸发时,都要用到的仪器是( )| A. | 烧杯 | B. | 玻璃棒 | C. | 蒸发皿 | D. | 酒精灯 |
分析 根据蒸发和过滤所需仪器即可找出共同需要的仪器.
解答 解:过滤需要铁架台、烧杯、漏斗、玻璃杯以及滤纸;蒸发需要铁架台(或三脚架)、蒸发皿、玻璃杯等仪器,则共同需要的仪器是玻璃棒.
故选B.
点评 本题考查分离所用仪器,题目难度不大,明确各操作所学仪器是解答该题的关键,注重相关基础知识的积累.

练习册系列答案
相关题目
7.通过比较相同时间内产生氧气的体积可探究影响过氧化氢分解速率的因素.
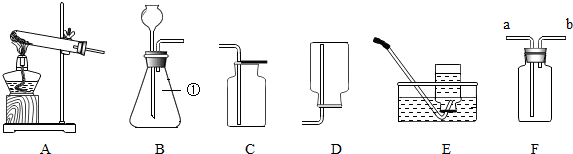
(1)用图1装置进行实验并绘制曲线图如图2.

写出实验I的化学反应方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,根据图1、图2信息可知,该因素对过氧化氢分解速率的影响是:在相同条件下,反应物的浓度越大,过氧化氢分解的速率越快.
(2)探究温度及催化剂质量的影响.请补填实验Ⅴ中的数据.
(3)溶液酸碱性对过氧化氢的分解速率也有影响,如图3:
①分析图3,可得出的结论是:在碱性溶液中过氧化氢的分解速率大于在酸性溶液中的分解速率,但不影响产物的最终质量.
②资料表明:过氧化钡(BaO2)与硫酸(H2SO4)溶液反应可用来制取H2O2,同时生成一种白色沉淀硫酸钡(BaSO4)该反应的化学方程式为:BaO2+H2SO4═H2O2+BaSO4↓;
从反应后的混合物中除去硫酸钡沉淀的实验操作是:过滤;根据①中结论可知,利用上述反应制取H2O2时,所加硫酸的量应:过量(填“少量”或“过量”).
(1)用图1装置进行实验并绘制曲线图如图2.

写出实验I的化学反应方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,根据图1、图2信息可知,该因素对过氧化氢分解速率的影响是:在相同条件下,反应物的浓度越大,过氧化氢分解的速率越快.
(2)探究温度及催化剂质量的影响.请补填实验Ⅴ中的数据.
| 实验编号 | 温度 | 催化剂 | 过氧化氢溶液的质量及浓度 |
| 实验Ⅲ | 50℃ | 1g二氧化锰 | 10g,3% |
| 实验Ⅳ | 25℃ | 2g二氧化锰 | 10g,3% |
| 实验Ⅴ | 25℃ | 2g二氧化锰 | 10g,3% |
①分析图3,可得出的结论是:在碱性溶液中过氧化氢的分解速率大于在酸性溶液中的分解速率,但不影响产物的最终质量.
②资料表明:过氧化钡(BaO2)与硫酸(H2SO4)溶液反应可用来制取H2O2,同时生成一种白色沉淀硫酸钡(BaSO4)该反应的化学方程式为:BaO2+H2SO4═H2O2+BaSO4↓;
从反应后的混合物中除去硫酸钡沉淀的实验操作是:过滤;根据①中结论可知,利用上述反应制取H2O2时,所加硫酸的量应:过量(填“少量”或“过量”).
9.下列反应属于化合反应的是( )
| A. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | B. | 乙炔+氧气 $\stackrel{点燃}{→}$水+二氧化碳 | ||
| C. | 铜锈$\stackrel{加热}{→}$ 氧化铜+水+二氧化碳 | D. | 锌+盐酸→氯化锌+氢气 |
6.下列物质的用途中,利用其物理性质的是( )
| A. | 生石灰用作干燥剂 | B. | 硫酸用于处理碱性废液 | ||
| C. | 氧气用于气焊 | D. | 干冰用作冷冻剂 |
7.下列图象能正确反映对应变化关系的是( )
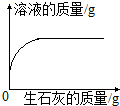 | 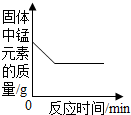 | 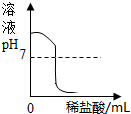 |  |
| A.一定质量的饱和石灰水中加入生石灰 | B.用酒精灯加热一定量的高锰酸钾固体 | C.向NaOH溶液中逐滴加入稀盐酸 | D.在一定量的CaCl2溶液中通入CO2气体 |
| A. | A | B. | B | C. | C | D. | D |