题目内容
锌和盐酸(HCl)反应生成氢气和氯化锌.实验室里用6.5g锌与足量的盐酸反应,可制得氢气和氯化锌的质量各是多少?
设可制得氢气质量为y,氯化锌的质量为x,
Zn+2HCl=ZnCl2+H2↑
65 136 2
6.5g x y
∴
=
,
=
,
解之得:y=0.2g,x=13.6g.
答:可制得H2质量为0.2g,可制得ZnCl2的质量为13.6g.
Zn+2HCl=ZnCl2+H2↑
65 136 2
6.5g x y
∴
| 65 |
| 2 |
| 6.5g |
| y |
| 65 |
| 136 |
| 6.5g |
| x |
解之得:y=0.2g,x=13.6g.
答:可制得H2质量为0.2g,可制得ZnCl2的质量为13.6g.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
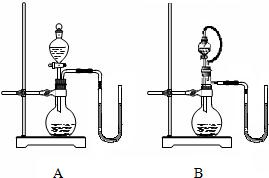 28、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
28、物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.


