题目内容
17.小明想配制某温度下的溶质质量分数为20%的氯化钾不饱和溶液100克.(1)他需要称量氯化钾的质量为多少克?水的质量为多少克?
(2)他加入8%的氯化钾溶液50克,溶液的质量分数又是多少?
(3)若向原溶液中加入16克氯化钾,该溶液达到饱和,求氯化钾在该温度下的溶解度.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)根据溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%,溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(3)溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量.
解答 解:(1)配制某温度下的溶质质量分数为20%的氯化钾不饱和溶液100克,溶质质量=溶液质量×溶质的质量分数,需氯化钾的质量=100g×20%=20g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-20g=80g.
(2)他加入8%的氯化钾溶液50克,溶液的质量分数又是$\frac{20g+50g×8%}{100g+50g}$×100%=16%.
(3)若向原溶液中加入16克氯化钾该溶液达到饱和,则即是该温度下80g水中溶解了20g+16g=36g氯化钾,则100g水中最多能溶解氯化钾的质量为36g×$\frac{100g}{80g}$=45g,溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量,则氯化钾在该温度下的溶解度为45g.
答:(1)需要称量氯化钾的质量为20g;水的质量为80g;
(2)溶液的质量分数又是16%;
(3)氯化钾在该温度下的溶解度为45g.
点评 本题难度不大,掌握溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%、溶质质量=溶液质量×溶质的质量分数是正确解答本题的关键.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
7.如图所示的实验仪器中,用来度量液体体积的是( )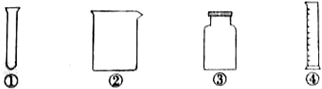

| A. | ① | B. | ② | C. | ③ | D. | ④ |
8.下列实验现象描述正确的是( )
| A. | 木炭在氧气中燃烧,发出白光,放热 | |
| B. | 红磷在空气中燃烧,产生大量白雾 | |
| C. | 铁丝在空气中燃烧,火星四射,生成黑色固体 | |
| D. | 镁带在空气中燃烧,发出耀眼的白光,生成氧化镁 |
5.“山水乐山”,“水”是乐山不可或缺的城市符号.爱乐山,就要爱护乐山的水资源.节约用水、防止水污染应成为我们的自觉行为.下列有关叙述,不正确的是( )
| A. | 过量排放含氮、磷元素的生活污水容易导致水体富营养化 | |
| B. | 农业生活中改变灌溉方式,变漫灌为喷灌或滴灌,以节约用水 | |
| C. | 城市生活污水、工业废水应遵循“先净化,后排放”的原则 | |
| D. | 采用燃烧氢气的方式生产水,以补充城市饮用水资源的不足 |
 如图所示实验是对人体呼出气体的主要成分进行的探究,如图所示
如图所示实验是对人体呼出气体的主要成分进行的探究,如图所示 Mg原子在化学反应中容易失去( 填“得到”或“失去”)2个电子.
Mg原子在化学反应中容易失去( 填“得到”或“失去”)2个电子. 下列图中微粒共表示3种元素,其中与氯原子具有相似化学性质的是D(填序号).
下列图中微粒共表示3种元素,其中与氯原子具有相似化学性质的是D(填序号).
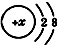 则x的数值可能是下列中的C、D.
则x的数值可能是下列中的C、D.