题目内容
某兴趣小组用如图13所示流程制取氧气(反应原理:2KClO3
2KCl+3O2↑).
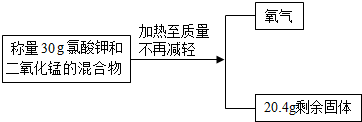
试计算:
(1)可制得氧气的质量为 g.
(2)根据化学方程式计算,原混合物中氯酸钾的质量?
| ||
| △ |

试计算:
(1)可制得氧气的质量为
(2)根据化学方程式计算,原混合物中氯酸钾的质量?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据质量守恒定律,即可求得氧气的质量;
(2)根据氧气的质量结合化学方程式即可计算氯酸钾的质量;
(2)根据氧气的质量结合化学方程式即可计算氯酸钾的质量;
解答:解:(1)依据质量守恒定律可知氧气的质量为30g-20.4g=9.6g;
(2)设原混合物中氯酸钾的质量为x.
2KClO3
2KCl+3O2↑
245 96
x 9.6g
=
,
x=24.5g
故答案为:(1)9.6;(2)答:原混合物中氯酸钾的质量为24.5g.
(2)设原混合物中氯酸钾的质量为x.
2KClO3
| ||
| △ |
245 96
x 9.6g
| 245 |
| x |
| 96 |
| 9.6g |
x=24.5g
故答案为:(1)9.6;(2)答:原混合物中氯酸钾的质量为24.5g.
点评:本题主要考查学生对物质质量守恒定律的认识以及利用化学方程式计算的能力,解题的关键是利用质量守恒定律求出氧气的质量.

练习册系列答案
相关题目
下列物质中,属于纯净物的是( )
| A、生铁 | B、石油 | C、金刚石 | D、空气 |
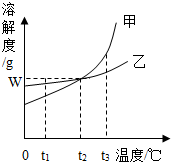 甲、乙两种物质的溶解度曲线如图所示.下列叙述错误的是( )
甲、乙两种物质的溶解度曲线如图所示.下列叙述错误的是( )| A、将甲、乙饱和溶液的温度从t2℃降到t1℃时,乙先析出晶体 |
| B、t1℃时,加入甲物质,可使不饱和的甲溶液变成饱和 |
| C、t1℃时,甲的溶解度小于乙的溶解度 |
| D、t2℃时,甲或乙两种物质饱和溶液中溶质与溶剂的比是W:100 |
2008年北京奥运火炬中使用的燃料是一种叫做丙烷(化学式为C3H8)的气体.下列说法中不正确的是( )
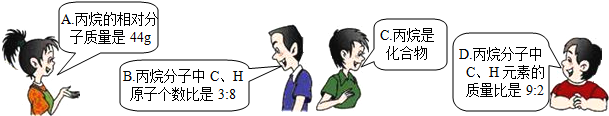

| A、A | B、B | C、C | D、D |
SiO2的读法是( )
| A、硅化二氧 | B、二氧化硅 |
| C、硅化氧 | D、氧化硅 |
下列对各种材料的开发利用过程中,主要过程属于化学变化的是( )
| A、用棉、麻等植物纤维纺纱织布 |
| B、用钛和钛合金制成飞机、火箭的外壳 |
| C、用 水、石灰石和纯碱等为原料生产烧碱 |
| D、用铝箔制成各种形状的制品 |