题目内容
18.有依据的猜想是科学家的基础,下列猜想合理的是( )| A. | 熟石灰常用于改良酸性土壤,所以烧碱也可以用于改良酸性土壤 | |
| B. | 稀硫酸能使紫色石蕊溶液变红,能使紫色石蕊变红的微粒可能是H2O、H+和SO42- | |
| C. | 氢氧化钠与稀盐酸充分反应后,所得溶液中的溶质可能有NaCl、NaOH、HCl | |
| D. | 石蜡是含碳、氢元素的混合物,石蜡燃烧可能生成CO、CO2、N2、H2O等产物 |
分析 A.根据物质的性质与用途来分析;
B.根据稀硫酸中含有的微粒来分析;
C.根据中和反应的过程来分析;
D.根据质量守恒定律来分析.
解答 解:A.烧碱具有很强的碱性和腐蚀性,不能用来改良酸性土壤,故错误;
B.稀硫酸中存在氢离子、硫酸根离子和水分子,所以可得出如上猜想,故正确;
C.氢氧化钠与稀盐酸完全充分反应后,只生成氯化钠和水,溶质只有氯化钠,故错误;
D.化学反应前后,元素的种类不变,石蜡是含碳、氢元素的混合物,燃烧后不可能生成氮气,故错误.
故选B.
点评 了解酸具有通性的原因;了解常见碱的性质和用途;掌握中和反应以及质量守恒定律,难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
8.下列化学用语与含义不相符的是( )
| A. | CO2-二氧化碳 | B. | 钙离子-Ca2+ | C. | 2个氧元素-2O | D. | 2个氢原子-2H |
6. 根据如图所示的溶解度曲线判断下列说法错误的是( )
根据如图所示的溶解度曲线判断下列说法错误的是( )
 根据如图所示的溶解度曲线判断下列说法错误的是( )
根据如图所示的溶解度曲线判断下列说法错误的是( )| A. | 20℃时A、C两物质的溶解度相等 | |
| B. | 升温可使C物质的不饱和溶液变饱和 | |
| C. | 50℃时把90gA物质放入100g水中能得到190g溶液 | |
| D. | 升温可使A物质的饱和溶液变不饱和 |
13.下列实验操作中,正确的是( )
| A. | 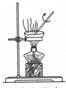 蒸发溶液 | B. |  量取溶液 | C. | 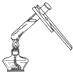 加热溶液 | D. |  滴加溶液 |
10.甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;丁:可能与氢氧化钠溶液质量分数大小有关.
【查阅资料】碳酸钠溶液显碱性.
【理论分析】
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象.
(2)乙同学的猜想也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试剂变红.
【实验设计】
(3)为证实丙同学的猜想,还需作如下实验,请完成下表.
(4)
(5)通过以上实验,四位同学看到:溶液先变成红色,一会儿红色又消失.因此酚酞红色褪去与氧气无关.若丁同学的猜想正确,设计如下实验证明并完成有关问题:
【猜想】甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;丁:可能与氢氧化钠溶液质量分数大小有关.
【查阅资料】碳酸钠溶液显碱性.
【理论分析】
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象.
(2)乙同学的猜想也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试剂变红.
【实验设计】
(3)为证实丙同学的猜想,还需作如下实验,请完成下表.
(4)
| 实验步骤 | 设计这一步骤的目的 |
| 1用煮沸过的蒸馏水配制氢氧化钠溶液. | |
| 2在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油. |
| 实验方法 | 观察到的现象和结论 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各滴加2滴酚酞试液. | 质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明 过浓的氢氧化钠也会使酚酞褪色. |
| 方案二: 将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释. | 溶液变红,说明与氢氧化钠溶液质量分数大小有关. |
7.以石油为原料的PX项目备受争议.PX学名对二甲苯,化学式为C8H10,广泛用于生产塑料、聚酯纤维和薄膜等.下列有关说法正确的是( )
| A. | 对二甲苯中碳、氢元素质量比为4:5 | |
| B. | 对二甲苯的相对分子质量为106g | |
| C. | 对二甲苯由8个碳原子、10个氢原子组成 | |
| D. | 塑料、聚酯纤维等属于有机高分子化合物 |