题目内容
将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
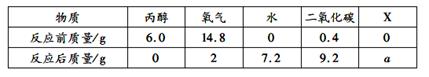
表中a的值为 ,参加反应的氧气和生成的二氧化碳的质量比为 ,X中一定含有 元素。
2.8 16:11 碳、氧
【解析】根据质量守恒定律,反应前后,物质的总质量不变,得6.0+14.8+0+0.4+0=0+2+
7.2+9.2+a,a=2.8;参加反应的氧气的质量为14.8g-2g=12.8g,生成的二氧化碳的质量为9.2g-0.4g=8.8g,参加反应的氧气和生成的二氧化碳的质量比为12.8g:8.8g=16:11;根据化学式中各元素的质量分数计算可得,丙醇中碳元素的质量为6.0g×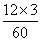 ×100%=3.6g,氢元素的质量为6.0g×
×100%=3.6g,氢元素的质量为6.0g×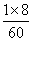 ×100%=0.8g,氧元素的质量为6.0g×
×100%=0.8g,氧元素的质量为6.0g×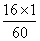 ×100%=1.6g,参加反应的氧气的质量为:14.8g-2g=12.8g,生成的水中氢元素的质量为:7.2g×
×100%=1.6g,参加反应的氧气的质量为:14.8g-2g=12.8g,生成的水中氢元素的质量为:7.2g×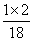 ×100%=0.8g,氧元素的质量为7.2g-0.8g=6.4g,二氧化碳中碳元素的质量为(9.2g-0.4g)×
×100%=0.8g,氧元素的质量为7.2g-0.8g=6.4g,二氧化碳中碳元素的质量为(9.2g-0.4g)×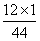 ×100%=2.4g,氧元素的质量为9.2g-0.4g-2.4g=6.4g,比较反应前后各元素的质量可知,X中一定含有碳、氧元素。
×100%=2.4g,氧元素的质量为9.2g-0.4g-2.4g=6.4g,比较反应前后各元素的质量可知,X中一定含有碳、氧元素。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)请从上表中查出关于碳元素的一条信息:___________________________
(2)第11号元素与第17号元素组成的化合物的化学式是 ,构成该物质的微粒是 (选填“分子”、“原子”或“离子”)。
(3)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填字母)。
A.C和Ne B.Be和Mg C.Al和Si D.F和Cl
下列实验指定容器中的水,其解释没有体现水的主要作用的是 ( )
| A | B | C | D | |
| 实 验 装 置 |
硫在氧气中燃烧 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
|
| 解释 | 集气瓶中的水: 吸收放出的热量 | 量筒中的水: 通过水体积的变化得出O2体积 | 集气瓶中的水: 冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:先将集气瓶内的空气排净,后便于观察H2何时收集满 |
 元素,下列有关说
元素,下列有关说 法错误的是( )
法错误的是( ) (2) 将t2℃时三种物质等质量的饱和溶液分别降温到0℃时,析出 溶质最多的是 ,无溶质析出的是 。
(2) 将t2℃时三种物质等质量的饱和溶液分别降温到0℃时,析出 溶质最多的是 ,无溶质析出的是 。 A.此实验的原理是利用铁生锈消耗氧气
A.此实验的原理是利用铁生锈消耗氧气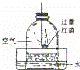


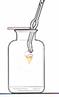
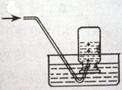 排水法收集氢气
排水法收集氢气 2CuO,测定“人造空气”中O2的含量
2CuO,测定“人造空气”中O2的含量