题目内容
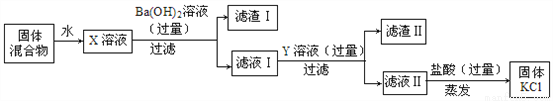
现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合液过滤后得到溶液的质量为140g。(反应的化学方程式为CaCl2+Na2CO3==CaCO3↓+2NaCl)
(1)生成沉淀的质量是 g。
(2)求碳酸钠溶液中溶质的质量分数是多少?
(1)10 (2)10.6% 【解析】试题分析:(1)根据题中的叙述可知生成的沉淀的质量为:50g+100g-140g=10g (2)碳酸钠溶液中溶质的质量分数是X CaCl2+Na2CO3==CaCO3↓+2NaCl 106 100 100g×X 10g 106/100=(100g×X) /10g X=10.6% 答:生成沉淀的质量为10g,碳酸钠...
练习册系列答案
相关题目


 自制白糖晶体 B.
自制白糖晶体 B. 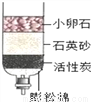 简易净水器净水
简易净水器净水 自制“叶脉书签” D.
自制“叶脉书签” D. 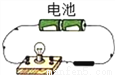 石墨导电实验
石墨导电实验