题目内容
9.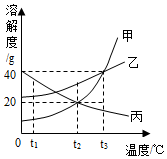 甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题;
甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题;①t1℃时,甲物质的溶解度<(填“>”“<”或“=”)丙物质的溶解度.
②t2℃时,将100g水加入到盛有15g甲物质的烧杯中,充分溶解后所得溶液时甲物质的不饱和溶液(填“饱和溶液”或“不饱和溶液”),该溶液的溶质质量分数13%.
③甲、乙、并三种物质的饱和溶液通过蒸发溶剂(方法)都能析出晶体.
④t3℃时,将甲、乙、丙三种物质的饱和溶液同时降温到t1℃,所得溶液的溶质质量分数由小到大的顺序是甲<丙<乙.
⑤t2℃时,某同学不能(填“能”或“不能”)用固体丙(不含结晶水)配制出50g溶质质量分数为20%的溶液,若不能,请写出原因t2℃时,丙物质饱和溶液的质量分数为16.7%..
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:①通过分析溶解度曲线可知,t1℃时,甲物质的溶解度<丙物质的溶解度;
②t2℃时,甲物质的溶解度是20g,所以将100g水加入到盛有15g甲物质的烧杯中,充分溶解后所得溶液时甲物质的不饱和溶液,该溶液的溶质质量分数为$\frac{15g}{115g}$×100%=13%;
③甲、乙、丙三种物质的饱和溶液通过蒸发溶剂都能析出晶体;
④t1℃时,乙物质的溶解度最大,降低温度,甲、乙物质会析出晶体,丙物质不会,t1℃乙物质的溶解度小于t3℃时丙物质的溶解度,所以t3℃时,将甲、乙、丙三种物质的饱和溶液同时降温到t1℃,所得溶液的溶质质量分数由小到大的顺序是甲<丙<乙;
⑤t2℃时,某同学不能用固体丙(不含结晶水)配制出50g溶质质量分数为20%的溶液,原因是:t2℃时,丙物质饱和溶液的质量分数为$\frac{20g}{120g}$×100%=16.7%.
故答案为:①<;
②不饱和溶液,13%;
③蒸发溶剂;
④甲<丙<乙;
⑤不能,t2℃时,丙物质饱和溶液的质量分数为16.7%.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
14.水是生命的源泉,也是不可缺少的资源.
(1)某矿泉水的主要矿物质成分机及含量如表,这里Ca、K、Zn、F是指元素.(填“单质、元素、分子或原子”)
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注,请参与讨论下列有关问题:
(Ⅰ)自来水、冰水混合物、海水中属于纯净物的是冰水混合物.
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:
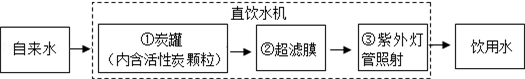
①对应的作用是B(填字母序号,下同).
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有AD.
A、工业废水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥、农药
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是AC.
A、氢气在氧气中燃烧生成水 B、水的蒸发 C、水的电解 D、水的净化
(3)长期饮用硬水可能会引起体内结石,鉴别硬水和软水最简单的方法是用肥皂水鉴别.
(4)水通电分解生成最理想的能源--氢气,电解一定量的水,当其中负极产生5ml气体时,正极产生的气体体积是2.5ml.
(1)某矿泉水的主要矿物质成分机及含量如表,这里Ca、K、Zn、F是指元素.(填“单质、元素、分子或原子”)
| 成分 | Ca | K | Zn | F |
| 含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
(Ⅰ)自来水、冰水混合物、海水中属于纯净物的是冰水混合物.
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:

①对应的作用是B(填字母序号,下同).
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有AD.
A、工业废水直接排放 B、工业废气处理后排放
C、禁止使用含磷洗衣粉 D、大量使用化肥、农药
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是AC.
A、氢气在氧气中燃烧生成水 B、水的蒸发 C、水的电解 D、水的净化
(3)长期饮用硬水可能会引起体内结石,鉴别硬水和软水最简单的方法是用肥皂水鉴别.
(4)水通电分解生成最理想的能源--氢气,电解一定量的水,当其中负极产生5ml气体时,正极产生的气体体积是2.5ml.
1.如图实验操作不正确的是( )
| A. | 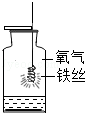 铁丝在氧气中燃烧 | B. | 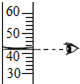 读取液体的体积 | ||
| C. | 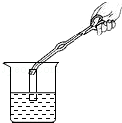 测溶液的PH | D. | 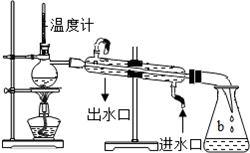 制取蒸馏水 |
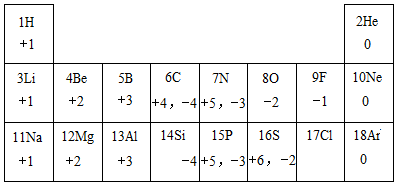 元素周期表是学习研究化学的重要工具.下表是1~18号元素的部分最高正价和最低负化合价规律信息:
元素周期表是学习研究化学的重要工具.下表是1~18号元素的部分最高正价和最低负化合价规律信息: