��Ŀ����
10�����Ķ����Ͽ����ش��й�����ͨ������£�������û����ɫ��û����ζ�����壬�ȿ����ᣬ��������ˮ��������ȼ�գ������ʵ�����Ʒ��ǣ�����ˮ�����ƺͼ�ʯ�����ֹ�̬ҩƷ������ĥ���Ȼ�Ϻ�װ���Թ��У����Ȳ����������壮
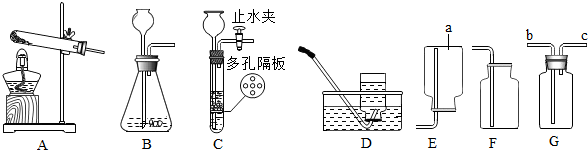
��1������a�������Ǽ���ƿ��
��2��д��ʵ������ȡCO2�Ļ�ѧ����ʽ��CaCO3+2HCl=CaCl2+H2O+CO2����
��3��ʵ������ȡ���ռ������װ����AD��AE������Ӧ��װ���Թ�ǰ��Ӧ�ȼ��װ�õ������ԣ���ȼ����ǰһ��Ҫ���鴿��
��4������Gװ�ò����ſշ��ռ�����������Ӧ��c������ѡ��b����c����
��5�����������ȼ���⣬����һ�ֺ���Ҫ�Ļ���ԭ�ϣ��ڴ����������£����Խ�COx��CH4�Ļ������ֱ��ת��Ϊ���ᣨCH3COOH�������÷�Ӧ��ԭ��������Ϊ100%����Ӧ���е�ԭ��ȫ��ת��ΪĿ������е�ԭ�ӣ�����COx�е�xΪ2���÷�Ӧ�����ǻ��Ϸ�Ӧ��
���� ��1��������������ƣ�
��2��ʵ���ҳ���ʯ��ʯ�����ʯ��ϡ���ᷴӦ��ȡ������̼��ͬʱ�����Ȼ��ơ�ˮ��д����Ӧ�Ļ�ѧ����ʽ���ɣ�
��3������ʵ������ȡ����ķ�Ӧ���ǹ��壬��Ӧ�����Ǽ��ȣ�������ܶȱȿ���С��������ˮ����ȡ����֮ǰ��Ҫ����װ�õ������ԣ���ȼ��ȼ������֮ǰ��Ҫ��������Ĵ��ȵ�֪ʶ���з�����
��4�������������ܶȱȿ���С��������
��5�����������غ㶨���Լ�������Ӧ���͵��жϷ������з�����
��� �⣺��1������a�������Ǽ���ƿ���������ƿ��
��2��ʵ���ҳ���ʯ��ʯ�����ʯ��ϡ���ᷴӦ��ȡ������̼��ͬʱ�����Ȼ��ơ�ˮ����Ӧ�Ļ�ѧ����ʽ�ǣ�CaCO3+2HCl=CaCl2+H2O+CO2�����ʴ�Ϊ��CaCO3+2HCl=CaCl2+H2O+CO2����
��3��ʵ������ȡ����ķ�Ӧ���ǹ��壬��Ӧ�����Ǽ��ȣ�������ܶȱȿ���С��������ˮ������ʵ������ȡ���ռ������װ�������AD��AE����ȡ����֮ǰ��Ҫ����װ�õ������ԣ���ȼ����ǰһ��Ҫ�ȼ������Ĵ��ȣ����AD��AE�������ԣ��鴿��
��4���������ܶȱȿ�����������װ��G�ռ�����ʱ�������Ӷ̹ܽ��룬���c��
��5���ڴ����������£����Խ�COx��CH4�Ļ������ֱ��ת��Ϊ���ᣨCH3COOH�������÷�Ӧ��ԭ��������Ϊ100%����COx�е�xΪ2���÷�Ӧ���㻯�Ϸ�Ӧ���һ���ص㣬���Է�Ӧ�����ǻ��Ϸ�Ӧ���ʴ�Ϊ��2�����Ϸ�Ӧ��
���� ������Ҫ���鳣������ķ���װ�����ռ�װ�õ�̽��������װ�����ݷ�Ӧ���״̬�ͷ�Ӧ����ѡ���ռ�װ������������ܶȺ��ܽ���ѡ��

 ��У����ϵ�д�
��У����ϵ�д�| A�� | 7.3% | B�� | 0.73% | C�� | 1.46% | D�� | ������ |
[�������1]������������Һ�Ƿ�������أ�
[ʵ��̽��1]
| ʵ����� | ʵ������ | ʵ����� |
| ȡ��������Һ���Թ��У�����Һ�еμ�ϡ���ᣬ�������� | ������ð���� | ����������Һһ�������ˣ� |
[���������]
����1������������Һ���ֱ��ʣ� ����2������������Һȫ�����ʣ�
[��������]��1���Ȼ�����Һ�����ԣ�
��2���Ȼ�����Һ����̼������Һ��Ӧ��CaCl2+Na2CO3=CaCO3��+2NaCl
[ʵ��̽��2]
| ʵ�鲽�� | ʵ������ | ʵ����� |
| ��1��ȡ��������Һ���Թ��У�����Һ�еμӹ������Ȼ�����Һ���������� | �а�ɫ�������ɣ� | ˵��ԭ��Һ��һ����̼���ƣ� |
| ��2��ȡ���裨1���Թ��е������ϲ���Һ���μӷ�̪��Һ�� | ��Һ���ɫ�� | ˵��ԭ��Һ��һ�����������ƣ� |
[��˼������]��1������������Һ¶���ڿ��������ױ��ʣ���д����ط�Ӧ�Ļ�ѧ����ʽ��CO2+2NaOH=Na2CO3+H2O��
��2��������[ʵ��̽��2]�У�С�������������������Һ�����Ȼ�����Һ������Ϊ�÷��������У�����С������С�����
[������Ӧ��]����������Һ���ױ��ʣ������ܷⱣ�森ʵ���ұ����ܷⱣ���ҩƷ���кܶ࣬������һ�����ӷ��Ե�ҩƷ��Ũ���ᡢ��ˮ�ȣ�������ˮ�Ե�ҩƷ��Ũ���ᡢ��ʯ�ң��������ʯ��ˮ��
| A�� | �ٽ����ȵ�ϸ��˿���������У�����ȼ�գ��������䣬���ɺ�ɫ���壻���������ջ�����ս���ëζ | |
| B�� | ���ڿ����е�ȼþ��������ҫ�۵İ⣬���ɺ�ɫ���壻�ں����ڿ�����ȼ�ղ����������� | |
| C�� | ����̼������Һ�еμӳ���ʯ��ˮ���а�ɫ��������������˿��������ͭ��Һ�����к�ɫ�������� | |
| D�� | ������������ȼ�ղ�������ɫ���棻��̼������Һ���뵽��ɫ��̪��Һ�У���ɫ��̪��Һ���ɫ |
| ִ�б���GB1413-99 ��Ҫ�ɷ֣�̼��� ��������ÿƬ����0.75g ÿƿ50Ƭ���� 40g ���������xx��˾��Ʒ�� |
��2��Ϊ�ⶨ����ʵ�ĺ�������С��ÿ��ȡ10Ƭ��Ƭ�����ѳ����ĺ�����������ձ��У������Ļ�ѧ��Ӧ�ǣ�CaCO3+2HCl=CaCl2+H2O+CO2������ַ�Ӧ���ٳ�ȡ�ձ���ʣ�������������С����������ʵ�飬�������£�
| ���ʵ����� | ��һ�� | �ڶ��� | ������ | ƽ��ֵ |
| ��Ӧǰ���ձ�+���� | 22g | 22g | 22g | 22g |
| 10Ƭ��Ƭ | 8g | 8g | 8g | 8g |
| ��Ӧ���ձ�ʮʣ���� | 26.7g | 26.5g | 26.9g | 26.7g |
| ѡ�� | �� �� | �� �� | �� �� |
| A | NaOH��Һ | Na2CO3 | ������������ |
| B | CO | CO2 | ͨ��ŨNaOH��Һ |
| C | CaCO3���� | CaO | �������� |
| D | KNO3��Һ | Ba��NO3��2��Һ | ����������Na2SO4��Һ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |