题目内容
10. 如图是某品牌尿素标签的一部分,下列有关尿素的说法中正确的是( )
如图是某品牌尿素标签的一部分,下列有关尿素的说法中正确的是( )| A. | 尿素属于复合肥料 | |
| B. | 尿素和熟石灰研磨有氨味 | |
| C. | 尿素中碳、氧、氮、氢的质量比是1:1:2:4 | |
| D. | 若杂质中不含氮元素,则这袋化肥中尿素的纯度约为98.6% |
分析 A、根据化学肥料的分类方法考虑;
B、根据铵态氮肥与碱性肥料反应产生氨气考虑;
C、根据元素质量的计算方法考虑;
D、根据元素质量分数的计算方法考虑.
解答 解:A、CO(NH2)2中含有氮元素,属于氮肥,故A错;
B、铵态氮肥与碱性肥料反应产生氨气,尿素中不含铵根离子,不能与熟石灰反应产生氨气,故B错;
C、CO(NH2)2中碳、氧、氮、氢四种元素的原子个数为1:1:2:4,而不是元素的质量比,故C错;
D、这袋化肥中尿素的纯度约为46%÷$\frac{28}{60}$≈98.6%,故D正确.
故选:D.
点评 氮磷钾这三种元素中只含有氮元素的是氮肥.只含有钾元素的是钾肥,只含有磷元素的是磷肥.含有两种或两种以上元素的化肥是复合肥.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
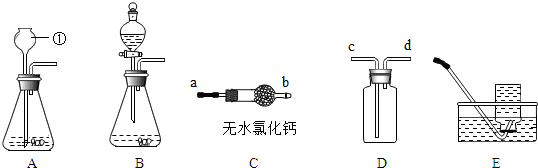
11.(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等.据此应将下列实验中的D与A(填“A”或“B”或“C”)归为一类,依据是D实验和A实验的主要目的都是探究物质的性质.
(2)我们已经学习过金属活动性的知识,知道金属活动性相对较强的金属能将活动性相对较弱的金属从其盐溶液中置换出来,根据此规律判断,Zn和Fe(NO3)2溶液能(填“能”或“不能”)反应,对于非金属,也有类似的规律,已知氯气(Cl2)的非金属活动性强于碘(I2),请写出氯气和碘化钾(KI)溶液反应的化学方程式Cl2+2KI=2KCl+I2.
 |  |
| A | B |
 |  |
| C | D |
15.下列图象正确的是( )
①表示KMnO4加热制O2生成的MnO2的质量与时间的关系图
②表示C还原CuO的实验中,试管内的固体质量与时间的关系图
③表示向CaCl2(含少量 HCl)溶液中滴加K2CO3溶液
④等质量的铁片和锌片分别和足量的质量分数相同的稀硫酸反应

①表示KMnO4加热制O2生成的MnO2的质量与时间的关系图
②表示C还原CuO的实验中,试管内的固体质量与时间的关系图
③表示向CaCl2(含少量 HCl)溶液中滴加K2CO3溶液
④等质量的铁片和锌片分别和足量的质量分数相同的稀硫酸反应

| A. | ①③ | B. | ③ | C. | ②④ | D. | ③④ |
2.能源已成为人们日益关注的话题.
(1)目前人们利用最多的能源是煤、石油和天然气等化石燃料,它们都是不可再生(填“可再生”或“不可再生”)能源,其中,被称为“工业的血液”的能源是石油.
(2)2014年南京青奥会火炬使用的燃料为A物质,纯净物A在B物质中充分燃烧,发生反应:A+5B=3C+4D(部分微观示意图如下所示).
①在上述反应中提供氧,具有氧化性的物质为O2.(填化学式)
②对于A物质的叙述正确的是D.
A、A物质由碳、氢、氧三种元素组成 B、A物质由碳、氧两种元素组成
C、A物质中碳、氢元素质量比是3:8 D、A物质的化学式是C3H8.
(1)目前人们利用最多的能源是煤、石油和天然气等化石燃料,它们都是不可再生(填“可再生”或“不可再生”)能源,其中,被称为“工业的血液”的能源是石油.
(2)2014年南京青奥会火炬使用的燃料为A物质,纯净物A在B物质中充分燃烧,发生反应:A+5B=3C+4D(部分微观示意图如下所示).
| 物质物质 | A | B | C | D |  |
| 分子示意图 | ? | 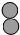 |  |  |
②对于A物质的叙述正确的是D.
A、A物质由碳、氢、氧三种元素组成 B、A物质由碳、氧两种元素组成
C、A物质中碳、氢元素质量比是3:8 D、A物质的化学式是C3H8.
19.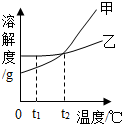 分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
(1)氯化钠的溶解度曲线是乙(填“甲”或“乙”).
(2)20℃时,将40gNH4Cl 加入100g 的水中,充分搅拌后得到的是饱和溶液(填“饱和”或“不饱和”),将上述溶液升温到30℃,该溶液的溶质质量分数为$\frac{40g}{100g+40g}$×100%(只列计算式,不需计算结果).
(3)如图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g水,析出晶体最多的是乙
(填“甲”或“乙”).
(4)计算配制50g 质量分数为3%的NaCl 溶液所需要质量分数为6%的NaCl溶液的体积,需要用到的数据是C.
A.3%的NaCl溶液的密度 B.水的密度 C.6%的NaCl溶液的密度.
 分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:
分析处理图表中的信息是学习化学的一种重要方法,运用溶解度表与溶解度曲线回答下列问题:| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)20℃时,将40gNH4Cl 加入100g 的水中,充分搅拌后得到的是饱和溶液(填“饱和”或“不饱和”),将上述溶液升温到30℃,该溶液的溶质质量分数为$\frac{40g}{100g+40g}$×100%(只列计算式,不需计算结果).
(3)如图,t1℃时,将两种物质的饱和溶液各100g,分别恒温蒸发5g水,析出晶体最多的是乙
(填“甲”或“乙”).
(4)计算配制50g 质量分数为3%的NaCl 溶液所需要质量分数为6%的NaCl溶液的体积,需要用到的数据是C.
A.3%的NaCl溶液的密度 B.水的密度 C.6%的NaCl溶液的密度.
20.下列图象能正确反映其对应关系的是( )
| A. |  加热一定质量的碳酸氢钠 | |
| B. | 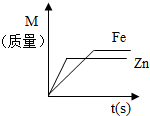 等量的锌、铁与足量的稀疏酸反应,产生氢气的质量M与反应时间t的关系图 | |
| C. | 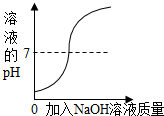 向一定体积的水中逐滴加入氢氧化钠溶液 | |
| D. | 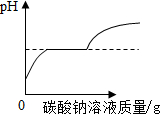 向一定量的盐酸和氯化钙的混合溶液中滴加碳酸钠溶液 |