题目内容
3.如表为元素周期表中某周期元素的原子结构示意图.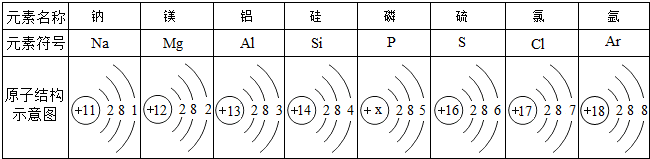 请回答下列问题:
请回答下列问题:(1)表中x为15;
(2)表中某元素的原子易得2个电子,其离子符号是S2-;
(3)由表中两种元素组成常见的AB2型化合物是氯化镁(写名称).
分析 (1)原子中,质子数=核外电子数,据此进行分析解答.
(2)根据原子结构示意图中最外层电子数来分析;
(3)根据原子结构示意图推测其在形成化合物时的化合价态,并书写化学式.
解答 解:(1)原子中,质子数=核外电子数,则x=2+8+5=15.故填:15;
(2)由原子结构示意图可知,硫原子最外层有6个电子,在化学反应中易得到2个电子而形成带两个单位负电荷的硫离子,故填:S2-;
(3)镁原子最外层有2个电子,易失去最外层的电子而显+2价,氯原子最外层有7个电子,易得到1个电子而显-1价,二者组成的化合物是氯化镁,化学式为MgCl2.故填:氯化镁.
点评 初中化学在物质结构部分出现了两种粒子结构示意图原子结构示意图和离子结构示意图.有关原子、离子结构示意图的题目要求知道图中各部分表示的意义熟悉核外电子排布的规律掌握原子结构中最外层电子数与元素性质的密切关系.这类试题考查的内容难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
14.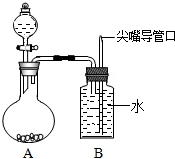 小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )
小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )
 小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )
小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )| A. | 氯化钠和水 | B. | 硝酸铵和水 | C. | 碳酸钙和稀盐酸 | D. | 铜和稀硫酸 |

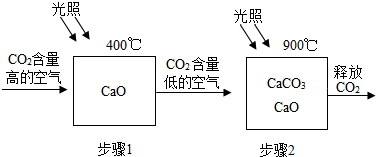

 按如图是细铁丝在氧气中燃烧的实验.
按如图是细铁丝在氧气中燃烧的实验.
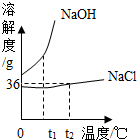 我国是海洋大国,浩瀚的海洋为我们提供了丰富的资源,为了保卫我们神圣的海权,近年来我国对南海部分岛礁进行了吹填扩建,为海洋资源的开发利用提供了便利条件.
我国是海洋大国,浩瀚的海洋为我们提供了丰富的资源,为了保卫我们神圣的海权,近年来我国对南海部分岛礁进行了吹填扩建,为海洋资源的开发利用提供了便利条件.