题目内容
8.某化工厂的废水中含有FeCL3(无其他杂质).小明同学采集了该废水样品,向其中滴加一定质量分数的NaOH溶液至溶液沉淀完成时消耗该NaOH溶液60g.待溶液冷至常温,将生成的沉淀滤出,经水洗,干燥后称重为10.7g,请计算所用NaOH溶质的质量分数.分析 氯化铁和氢氧化钠反应生成氢氧化铁沉淀和氯化钠,根据沉淀氢氧化铁的质量可以计算氢氧化钠的质量,进一步可以计算所用NaOH溶质的质量分数.
解答 解:设反应的氢氧化钠质量为x,
FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
120 107
x 10.7g
$\frac{120}{x}$=$\frac{107}{10.7g}$,
x=12g,
所用NaOH溶质的质量分数为:$\frac{12g}{60g}$×100%=20%,
答:所用NaOH溶质的质量分数为20%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
18.不属于溶液的是( )
| A. | 啤酒 | B. | 可口可乐 | C. | 矿泉水 | D. | 蒸馏水 |
19.物质分散在水中,经搅拌过滤后,所得溶液名称正确的是( )
| A. | 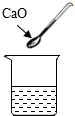 氧化钙溶液 | B. | 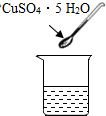 胆矾溶液 | C. | 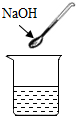 纯碱溶液 | D. | 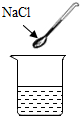 食盐溶液 |
16.下列实验现象的描述正确的是( )
| A. | 红磷在空气中燃烧:产生黄白色火焰,生成大量白色五氧化二磷 | |
| B. | 硫在氧气中燃烧:发出淡蓝色火焰,产生有刺激性气味的气体 | |
| C. | 一氧化碳还原氧化铁粉末:黑色固体变为银白色,澄清石灰水变浑浊 | |
| D. | 熟石灰与氯化铵混合研磨:白色固体中产生具有刺激性气味的气体 |
3.某溶液中滴加BaCl2溶液,产生白色沉淀,以下判断正确的是( )
| A. | 一定是硫酸 | B. | 一定含有硫酸根 | C. | 一定是碳酸钠 | D. | 以上结论都错误 |
7.下列除去杂质的方法中,正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | Cu(NO3)2和(AgNO3) | 加过量铜粉,过滤 |
| B | KCL溶液(CaCl2) | 加适量Na2CO3溶液,过滤 |
| C | CuO(Cu) | 滴加足量稀盐酸,过滤 |
| D | HCl(水蒸气) | 将气体通过生石灰 |
| A. | A | B. | B | C. | C | D. | D |
8.在配置氢氧化钠溶液的操作中正确的是( )
| A. |  称取NaOH固体 | B. |  量取一定量的水 | C. |  溶解 | D. |  装瓶 |
