题目内容
13.某食盐样品中含有少量沙土、氯化钙和氯化镁等杂质.以下是除去食盐样品中杂质的实验流程,根据流程图回答:
(1)操作A的名称是过滤;
(2)加入的试剂B是稀盐酸(填名称);
(3)加入NaOH时发生反应的化学方程式:2NaOH+MgCl2=Mg(OH)2↓+2NaCl(不考虑生成微溶物可能形成的沉淀).
分析 (1)操作A是将沉淀与滤液分离,进行分析解答.
(2)氢氧化钠能与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,过滤后的滤液中含有氯化钠、过量的氢氧化钠和碳酸钠,进行分析解答.
(3)加入NaOH时,氢氧化钠能与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,写出反应的化学方程式即可.
解答 解:(1)操作A是将沉淀与滤液分离,故操作A的名称是过滤.
(2)氢氧化钠能与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,过滤后的滤液中含有氯化钠、过量的氢氧化钠和碳酸钠,氢氧化钠、碳酸钠均能与稀盐酸反应,分别生成氯化钠和水,氯化钠、水和二氧化碳,能除去过量的杂质,故加入的试剂B是稀盐酸.
(3)加入NaOH时,氢氧化钠能与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,反应的化学方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
故答案为:(1)过滤;(2)稀盐酸;(3)2NaOH+MgCl2=Mg(OH)2↓+2NaCl.
点评 本题难度较大,考查了氯化钠提纯中离子的除杂,除去多种杂质离子时,往往要考虑除杂的顺序、后面加入的试剂要能除去前面加入的过量的试剂.

练习册系列答案
相关题目
3.已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如下,则下列说法中,正确的是( )

(说明:一种小球代表一种元素的原子)

(说明:一种小球代表一种元素的原子)
| A. | 图中的反应物都是化合物 | B. | 该反应属于置换反应 | ||
| C. | 该反应中没有元素化合价改变 | D. | 该反应不符合质量守恒定律 |
2.如表是活禽市场某种消毒液的主要成分:
请根据此表,将下列带点部分的内容用恰当的化学用语填写在横线上:
(1)该消毒液的溶剂H2O;
(2)该消毒液中含有的金属离子Ag+;
(3)标注硝酸中氮元素的化合价H$\stackrel{+5}{N}$O3.
| 用 途 | 杀菌消毒 |
| 主要成分 | 硝酸、硝酸银、过氧化氢 |
(1)该消毒液的溶剂H2O;
(2)该消毒液中含有的金属离子Ag+;
(3)标注硝酸中氮元素的化合价H$\stackrel{+5}{N}$O3.
 小政同学在复习Ca(OH)2化学性质时,归纳出了Ca(OH)2与其它物质间相互反应的关系如图(图中“--”表示相连的两种物质能发生反应).
小政同学在复习Ca(OH)2化学性质时,归纳出了Ca(OH)2与其它物质间相互反应的关系如图(图中“--”表示相连的两种物质能发生反应).
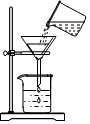 将含有少量泥沙的食盐提纯并配制食盐水溶液,某同学进行以下实验操作,回答下列问题.
将含有少量泥沙的食盐提纯并配制食盐水溶液,某同学进行以下实验操作,回答下列问题.