题目内容
4.炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生成CuCl2的流程图如图: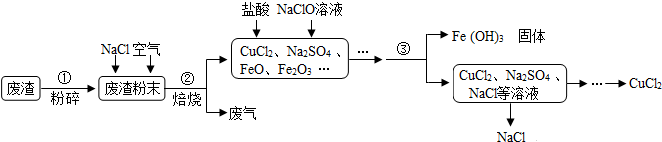
(1)操作2的名称是过滤.
(2)操作1中将废渣变成粉末的目的是增大反应物的接触面积.
(3)CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4.其化学方程式为;CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4.
(4)流程图中能循环利用的物质是NaCl.Fe元素的化合价有3种.
分析 (1)操作2是将氢氧化铁固体与溶液分离,进行分析解答.
(2)操作1中将废渣变成粉末,能增大接触面积,进行分析解答.
(3)CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4,写出反应的化学方程式即可.
(4)根据既是反应物,也是生成物的物质,可以循环使用进行分析解答.
根据单质中元素的化合价为0,在化合物中正负化合价代数和为零,结合含有铁元素的物质,进行分析解答.
解答 解:(1)操作2是将氢氧化铁固体与溶液分离,操作2的名称是过滤.
(2)操作1中将废渣变成粉末,能增大反应物的接触面积,利于反应的进行.
(3)CuS、NaCl和O2在高温条件下反应生成CuCl2和Na2SO4,反应的化学方程式为:CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4.
(4)由流程可知,反应过程中加入了氯化钠,最后又生成了氯化钠,所以循环利用的物质是NaCl.
铁属于单质,铁元素的化合价为0;含铁的化合物由FeO、Fe2O3、Fe(OH)3,铁元素的化合价分别是+2、+3、+3,故Fe元素的化合价有3种.
故答案为:(1)过滤;(2)增大反应物的接触面积;(3)CuS+2NaCl+2O2$\frac{\underline{\;高温\;}}{\;}$CuCl2+Na2SO4;(4)NaCl;3.
点评 本题难度不大,理解工业上废渣为原料生成CuCl2的流程图,掌握过滤、化学方程式的书写方法、化合价的原则等是正确解答本题的关键.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
12.a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
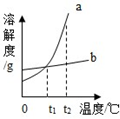

| A. | 将t1℃时b 的饱和溶液升温到t2℃,溶液质量不变 | |
| B. | 将t2℃时a 的饱和溶液降温至t1℃,溶液质量减小 | |
| C. | t2℃时,两种物质的溶液中溶质的质量分数a 一定大于b | |
| D. | t2℃时,两种物质的饱和溶液分别降温至t1℃,两溶液溶质的质量分数相等 |
13.下列图象不能正确反映对应的反应过程的是( )
| A. | 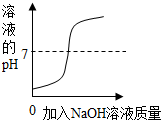 向一定质量的氢氧化钠溶液中逐滴加入稀盐酸 | |
| B. | 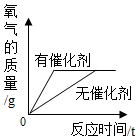 用一定量的过氧化氢制取氧气 | |
| C. | 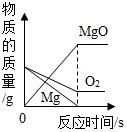 等质量的镁和氧气在点燃的条件下充分反应 | |
| D. | 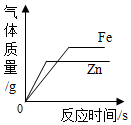 相同质量的铁粉和锌粉分别放入足量稀盐酸中 |
14.下列物质的用途与化学反应原理及反应类型对应不相符的是( )
| A. | 用高锰酸钾制取氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ 分解反应 | |
| B. | 用生石灰做食品干燥剂:CaO+H2O=Ca(OH)2 化合反应 | |
| C. | 用Al(OH)3治疗胃酸过多:Al(OH)3+3HCl=AlCl3+3H2O 复分解反应 | |
| D. | CO用于炼铁:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 |
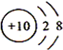 所示的粒子构成的单质Ne.
所示的粒子构成的单质Ne.
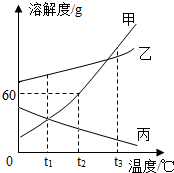 甲、乙、丙三种固体物质的溶解度曲线如图所示,请根据图示回答下列问题.
甲、乙、丙三种固体物质的溶解度曲线如图所示,请根据图示回答下列问题.