题目内容
15gA物质与5gB物质恰好完全反应,生成6gC物质和若干D物质,若要生成7gD物质,则需要A物质( )
| A、8g | B、7.5g |
| C、15g | D、14g |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:由反应A+B═C+D中,由5gA与2gB恰好完全反应生成3gC,根据质量守恒定律,可计算生成D物质的质量,判断反应中A、D物质质量关系,由反应有8gD生成可计算物质A的质量.
解答:解:
根据质量守恒定律,反应A+B═C+D中,15gA与5gB恰好完全反应生成6gC时,生成D物质质量=15g+5g-6g=14g,则反应中物质A、D的质量比=15g:14g=15:14;
则当反应有7gD生成时,参加反应的A质量=7g×
=7.5g.
故选:B.
根据质量守恒定律,反应A+B═C+D中,15gA与5gB恰好完全反应生成6gC时,生成D物质质量=15g+5g-6g=14g,则反应中物质A、D的质量比=15g:14g=15:14;
则当反应有7gD生成时,参加反应的A质量=7g×
| 15 |
| 14 |
故选:B.
点评:对于此无具体反应化学方程式的计算,首先由反应中各物质的质量确定反应中物质的质量比,是解决问题的基本思路.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
在一个密闭的容器内有甲、乙、丙、丁四种物质,通过电火花引燃后,充分反应.经测定,容器内反应前后各物质的质量如下:
若甲的相对分子质量为n,丁的相对分子质量为2n,则下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 4 | 10 | 1 | 25 |
| 反应后质量/g | 未测 | 21 | 10 | 9 |
| A、该反应一定是置换反应 |
| B、该反应中甲与丁的化学计量数之比为1:2 |
| C、甲反应后的质量为4g |
| D、该反应中生成乙与丙的质量比为21:10 |
碘是人体必需的微量元素之一.下列说法错误的是( )
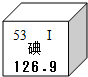

| A、碘的元素符号是I |
| B、碘原子的中子数为53 |
| C、碘元素的相对原子质量为126.9 |
| D、碘原子的核外电子数为53 |
下列图示的实验操作正确的是( )
A、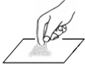 取用药品 |
B、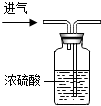 干燥氧气 |
C、 闻气体的气味 |
D、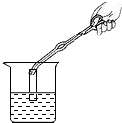 测定溶液的pH |
我国南海海底温藏着丰富的锰结核含有锰、铁、铜等金属的矿物.已知铜原子的核内质子数为29,相对原子质量为64,则铜原子的核外电子数为( )
| A、29 | B、35 | C、64 | D、93 |
下列实验现象的描述与相应化学方程式的书写都正确的是( )
| A、镁条插入硫酸铜溶液,镁条表面出现红色物质:Mg+CuSO4=MgSO4+Cu | ||||
B、铁丝在空气中剧烈燃烧,火星四射生成黑色固体:3Fe+2O2
| ||||
| C、水受热至沸腾,产生水蒸气:2H2O=2H2↑+O2↑ | ||||
| D、烤羊肉串时,看到木炭发红光,放出大量的热:C+O2=CO2 |
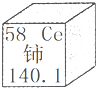 我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获2008年度“国家最高科学技术奖”.铈(Ce)是一种常见的稀土元素,下列关于铈的说法正确的是( )
我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获2008年度“国家最高科学技术奖”.铈(Ce)是一种常见的稀土元素,下列关于铈的说法正确的是( )| A、中子数是58 |
| B、相对原子质量58 |
| C、铈元素是金属元素 |
据报道,1994年12月科学家发现一种新元素,它的相对原子质量为271,其原子核内有158个中子.该元素的核电荷数为( )
| A、433 | B、161 |
| C、272 | D、113 |
 化学是研究物质的结构、性质以及变化规律的科学,研究元素知识是学好化学的基础.下包含部分元素的相关信息,完成以下填空:
化学是研究物质的结构、性质以及变化规律的科学,研究元素知识是学好化学的基础.下包含部分元素的相关信息,完成以下填空: