题目内容
14.利用化学反应中气体产生的压力,可使多个化学反应依次发生,根据图示回答下列问题(A装置中的试剂足量,B、C、D中的试剂少量):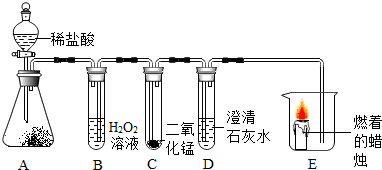
(1)打开A中分液漏斗的活塞,使稀盐酸逐滴滴下,A中的反应方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O.
(2)B中观察到的现象是试管内液体沿导管流出.
(3)C中发生反应的方程式开始从导管流入的液体遇黑色粉末产生气泡,后来产生的气泡越来越少,从导管内有气泡冒出.
(4)D中发生反应的方程式CO2+Ca(OH)2═CaCO3↓+H2O.
(5)E中的现象是蜡烛先明亮后熄灭.
分析 (1)A中的稀盐酸与大理石反应生成碳酸钙、水、二氧化碳,我们可以根据反应物和生成物写出化学反应式;
(2)A中生成的气体沿导管进入B,在大气压力的作用下,B中的液体沿长导管流出;
(3)开始B中的H2O2溶液进入C,与C中的二氧化锰反应生成气体;因试剂少量,后来不能再生成气体;
(4)因C中的试剂少量,(1)中生成的二氧化碳气体会有剩余,剩余的气体进入D,与澄清石灰水反应.据此写出化学反应式;
(5)D中澄清石灰水的量也不足,剩余的二氧化碳气体进入E,使蜡烛熄灭.
解答 解:(1)A中的反应物是稀盐酸和大理石,生成物是碳酸钙、水、二氧化碳.化学反应式是:CaCO3+2HCl═CaCl2+CO2↑+H2O.故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O;
(2)A中生成的二氧化碳气体进入B,在大气压强的作用下B中的H2O2溶液沿导管进入C,故答案为:试管内液体沿导管流出;
(3)进入C的H2O2溶液在二氧化锰催化作用下反应生成氧气,所以开始可以看到流入的液体遇黑色粉末产生气泡,双氧水反应完后,不再有气泡产生,从导管内有气泡冒出.
故答案为:开始从导管流入的液体遇黑色粉末产生气泡,后来产生的气泡越来越少,从导管内有气泡冒出;
(4)A、C中生成的气体进入D后,A中生成的二氧化碳气体可以使澄清的石灰水变浑浊.化学反应式是:CO2+Ca(OH)2═CaCO3↓+H2O.
故答案为:CO2+Ca(OH)2═CaCO3↓+H2O;
(5)因D中的试剂少量,所以二氧化碳气体没有充分反应,并沿导管进入E.二氧化碳不支持燃烧,所以进入E的二氧化碳气体使蜡烛熄灭.故答案为:蜡烛先明亮后熄灭.
点评 本题主要考查化学方程式的书写、二氧化碳的性质,要同学们熟悉常见化学反应以及常见气体的性质.

| A. | 2O | B. | O2 | C. | O2- | D. | O22- |
| A. | 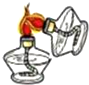 | B. |  | C. |  | D. | 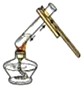 |
| A. | pH试纸 | B. | 石蕊溶液 | C. | 酚酞溶液 | D. | 温度计 |
| A. | 钢铁生锈 | B. | 食物腐败 | C. | 汽车轮胎爆炸 | D. | 烧制陶器 |
| A. | 分子的质量和体积都很小 | B. | 分子在不断地运动 | ||
| C. | 分子是由原子构成的 | D. | 分子之间存在间隔 |