题目内容
3. 两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.【提出问题】这两瓶黑色粉末A和B分别是什么物质?
【猜想】甲同学:A是铁粉,B是二氧化锰.
乙同学:A是炭粉,B是氧化铜.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是铁粉. |
| ②取少量B粉末于试管中,加入适量稀硫酸. | 黑色粉末溶解,溶液显蓝色. | B粉末是氧化铜. 反应方程式为CuO+H2SO4=CuSO4+H2O. |
(1)乙同学的猜想正确.
(2)通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是增大反应物的接触面积,使反应更充分;
同学们按如图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时,不能(填写“可以”或者“不能”)确定氧化铜和炭粉已经开始反应;实验结束时,先将导管移出,再熄灭酒精灯的原因是
防止液体倒吸炸裂试管.
(3)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例,你建议选择A(填写字母),简要说明你的理由反应中炭粉会与试管内的氧气反应而部分消耗,故稍过量的炭粉有利于反应的进行.
A.36:3 B.40:3 C.48:3.
分析 【实验探究】铁能和稀硫酸反应生成硫酸亚铁和氢气,碳不能和稀硫酸反应;
氧化铜和稀硫酸反应生成硫酸铜和水,硫酸铜溶液是蓝色的;
【反思与拓展】反应物接触面积越大,反应速率越快,反应越充分;
按如图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时,不能确定氧化铜和炭粉已经开始反应,这是因为加热时,试管中的二氧化碳气体进入澄清石灰水中,能使澄清石灰水变浑浊,炭粉能和试管中的氧气反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊;
为了防止液体倒吸炸裂试管,实验结束时,应该先将导管移出,再熄灭酒精灯;
高温条件下,氧化铜和碳反应生成铜和二氧化碳,根据反应的化学方程式及其质量关系可以判断相关方面的问题.
解答 解:【实验探究】①取少量A粉末于试管中,加入适量稀硫酸,黑色粉末不溶解,没有气体产生,A粉末一定不是铁粉,这是因为如果是铁粉,则铁粉由于和稀硫酸反应而溶解,并且产生气泡;
②取少量B粉末于试管中,加入适量稀硫酸,黑色粉末溶解,溶液显蓝色,B粉末是氧化铜,氧化铜和稀硫酸反应生成硫酸铜和水,反应的化学方程式为:
CuO+H2SO4=CuSO4+H2O,实验过程如下表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量A粉末于试管中,加入适量稀硫酸. | 黑色粉末不溶解,没有气体产生. | A粉末一定不是铁粉. |
| ②取少量B粉末于试管中,加入适量稀硫酸. | 黑色粉末溶解,溶液显蓝色. | B粉末是氧化铜. 反应方程式为CuO+H2SO4=CuSO4+H2O. |
(2)用超细炭粉与氧化铜粉末混合进行实验,能够增大反应物的接触面积,使反应更充分;
按如图装置进行实验,当看到澄清的石灰水刚刚出现浑浊时,不能确定氧化铜和炭粉已经开始反应,这是因为加热时,试管中的二氧化碳气体进入澄清石灰水中,能使澄清石灰水变浑浊,炭粉能和试管中的氧气反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊;
实验结束时,先将导管移出,再熄灭酒精灯,能够防止液体倒吸炸裂试管.
故填:增大反应物的接触面积,使反应更充分;不能;防止液体倒吸炸裂试管.
(3)氧化铜和碳在高温条件下反应生成铜和二氧化碳,反应的化学方程式及其质量关系为:
2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,
160 12
由以上质量关系可知,氧化铜和碳恰好完全反应时的质量比为:160:12=40:3,为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和炭粉的质量比例,应该选择36:3,这是因为反应中炭粉会与试管内的氧气反应而部分消耗,故稍过量的炭粉有利于反应的进行.
故填:A;反应中炭粉会与试管内的氧气反应而部分消耗,故稍过量的炭粉有利于反应的进行.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
13.下列化学符号所表示的意义错误的是( )
| A. | H2:可以表示一个氢气分子 | B. | Cu2+:可以表示铜单质 | ||
| C. | S:可以表示一个硫原子 | D. | H2O:可以表示水这种物质 |
14.下列与化学有关的知识内容正确的是( )
| A. | H2、CH4都是可燃气体--点燃前须检验纯度 | |
| B. | 水污染--对人类没有影响 | |
| C. | 油锅着火时用水浇灭 | |
| D. | 鉴别硝酸铵和硫酸铵--加熟石灰研磨,闻气味 |
11.根据如表回答相关问题.
①表中两种物质的溶解度相等的温度范围是在20~40℃.
②20℃时,硝酸钾的溶解度是31.6g/100g水,其含义是20℃时100g水中溶解31.6g硝酸钾达到饱和.该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是65.8g.要进一步提高该溶液的溶质质量分数,可进行的操作是加热.
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是冷却热饱和溶液.
④60℃时,对100g硝酸钾饱和溶液(如A烧杯)进行如下操作,请回答相关问题:

上述溶液中所含溶质的质量D=E(填“>”或“<”或“=”,下同),溶液不饱和的是 C(用A、B、C、D、E填空),溶液B、C、E中溶质质量分数的大小关系是B=E>C.
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度(g/100g水) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
②20℃时,硝酸钾的溶解度是31.6g/100g水,其含义是20℃时100g水中溶解31.6g硝酸钾达到饱和.该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是65.8g.要进一步提高该溶液的溶质质量分数,可进行的操作是加热.
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是冷却热饱和溶液.
④60℃时,对100g硝酸钾饱和溶液(如A烧杯)进行如下操作,请回答相关问题:

上述溶液中所含溶质的质量D=E(填“>”或“<”或“=”,下同),溶液不饱和的是 C(用A、B、C、D、E填空),溶液B、C、E中溶质质量分数的大小关系是B=E>C.
8.化学在环境保护、资源和能源利用等方面起着重要的作用,下列说法正确的是( )
| A. | 防止金属腐蚀是保护金属资源的唯一途径 | |
| B. | 煤、石油、天然气都属于不可再生的化石燃料 | |
| C. | 天然水经过沉降、过滤、吸附、消毒,得到的是纯水 | |
| D. | 目前计入空气污染指数的有害气体主要包括:SO2、CO2、NO2、臭氧等 |
15.酚酞(C20H14O4)是实验室常用的指示剂,下列有关说法正确的是( )
| A. | 酚酞的相对分子质量为318g | |
| B. | 酚酞是由20个碳原子、14个氢原子和4个氧原子构成 | |
| C. | 酚酞中碳、氢、氧元素的质量比为20:14:4 | |
| D. | 酚酞中碳元素的质量分数最大 |
12.下列实验操作中,能达到实验目的是( )
| A. |  干燥氨气 | B. | 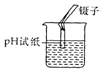 测定某溶液的pH | ||
| C. | 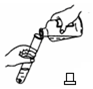 向试管中倾倒液体 | D. | 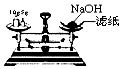 称取氢氧化钠固体 |
13.已知某两种物质在一定条件下发生化学反应,其微观示意图如下,下列说法正确的是( )
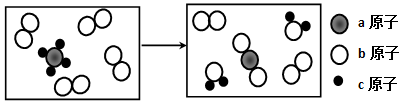

| A. | 反应前后分子的种类、个数都发生改变 | |
| B. | 该反应不是置换反应 | |
| C. | 参加反应的两种分子的个数比为4:1 | |
| D. | 该反应中生成物有单质和化合物 |