题目内容
17. 如图是实验室用大理石和稀盐酸制取二氧化碳的实验装置图,请回答:
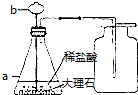
如图是实验室用大理石和稀盐酸制取二氧化碳的实验装置图,请回答:(1)仪器a的名称是锥形瓶,仪器b的名称是长颈漏斗;
(2)用向上排空气法收集二氧化碳气体的原因是密度比空气的大,能溶于水;
(3)将146g10%的稀盐酸和足量的大理石完全反应,可产生二氧化碳8.8克.
分析 (1)根据常见的化学仪器的名称进行分析解答.
(2)根据二氧化碳的密度及水溶性来选择收集装置,进行分析解答.
(3)根据参加反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式列式计算出生成二氧化碳的质量即可.
解答 解:(1)仪器a是锥形瓶;仪器b是长颈漏斗.
(2)二氧化碳密度比空气的大,能溶于水,所以应该选择向上排空气法来收集二氧化碳.
(3)设生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
146g×10% x
$\frac{73}{44}=\frac{146g×10%}{x}$ x=8.8g.
故答案为:(1)锥形瓶;长颈漏斗;(2)密度比空气的大,能溶于水;(3)8.8.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据、利用化学方程式的有关计算等是正确解答本题的关键.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
7.对比归纳是学习化学的重要方法,请你参与下列探究活动并回答问题:
【探究活动一】探究影响物质溶解性的因素.
【探究活动二】比价氯化铁固体和硫酸铜固体对过氧化氢溶液分解的催化效果
【探究活动三】探究影响木炭燃烧剧烈程度的因素.
【探究活动四】研究二氧化碳能否与碱溶液的反应.
【探究活动一】探究影响物质溶解性的因素.
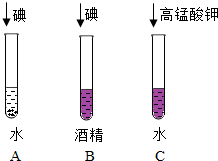 | ①同学们做了如图所示A试管和B试管的对比实验,发现B中固体可溶,A中几乎不溶,该对比实验说明了影响物质溶解性的因素是溶剂的种类; ②同学们又补充了C试管所示实验,他们想探究的影响因素是溶质的种类. |
 | ①实验中需要控制的变量除了氯化铁和硫酸铜的质量、过氧化氢溶液的体积,还有温度、过氧化氢溶液的溶质质量分数(填两条) ②可通过观察产生气泡的速率来定性比较两者的催化效果. |
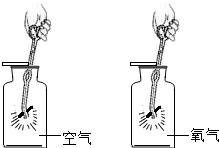 | 木炭在氧气里燃烧比在空气里燃烧更剧烈,说明了影响木炭燃烧剧烈程度的因素是氧气的浓度. |
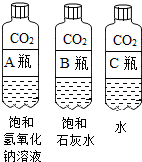 | ①分别震荡三个软质塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O. ②对比A瓶与C瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应. |
8.根据你的生活经验和所学的化学知识,判断下列做法正确的是( )
| A. | 用钢丝球洗刷铝制炊具 | |
| B. | 食品袋里充入氮气延长食品的保质期 | |
| C. | 服用熟石灰治疗胃酸过多症 | |
| D. | 高层住房着火时,立即乘电梯撤离 |
12.下列生活实例中,其过程主要属于化学变化的是( )
| A. | 淘米洗菜 | B. | 水果榨汁 | C. | 粮食酿酒 | D. | 小麦磨面 |
2.下列实验方案中,可行的是( )
| A. | 用细铁丝在密闭容器中燃烧,除尽密闭容器内空气中的氧气 | |
| B. | 向某种溶液中加入氯化钡溶液,产生白色沉淀,证明该溶液一定是硫酸盐 | |
| C. | 按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物 | |
| D. | 用玻璃棒蘸取食用白醋滴在润湿pH试纸上,测定其pH |
9.下列对实验结果推测正确的是( )
| A. | 无色气体在空气中燃烧产生蓝色火焰,说明气体是甲烷 | |
| B. | 某固体中加入稀盐酸,产生无色,无味的气体,该固体中不一定含有CO32- | |
| C. | 往溶液中滴加氯化钡溶液有白色沉淀,该沉淀一定是BaSO4 | |
| D. | 某无色溶液中滴入无色酚酞试液,显无色,该溶液一定不是酸溶液 |
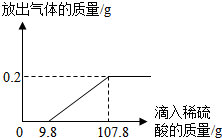 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题: