题目内容
20.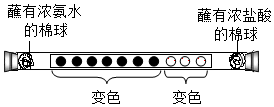 取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象,则下列说法中正确的是( )
取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象,则下列说法中正确的是( )| A. | 该过程中没有化学反应发生 | |
| B. | 所有气体分子的运动速率都相同 | |
| C. | 图示黑点表示石蕊溶液变成了红色 | |
| D. | 图示小白圈表示石蕊溶液变成了红色 |
分析 根据已有的分子运动以及酸碱指示剂在酸碱溶液中的变色的知识进行分析解答即可.
解答 解:
A、该过程中氨气和氯化氢反应生成了氯化铵,产生了新物质,发生了化学变化,错误;
B、据图可以看出,氨水这边变色的滴数是7滴,浓盐酸这边的滴数是3滴,故氨气的运动速率大于氯化氢,说明分子的运动速率不同,错误;
C、氨水呈碱性,能使石蕊试液变蓝,不是红色,错误;
D、盐酸显酸性,能是紫色石蕊溶液变红,正确.
故选:D.
点评 本题考查的是常见的酸和碱的挥发性以及酸碱指示剂变色的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
11.生铁和足量的稀盐酸充分反应后,总会有一些残渣剩余,残渣的成分主要是( )
| A. | 碳 | B. | 氯化铁 | C. | 氯化亚铁 | D. | 铁 |
8.如图为元素周期表第4周期的一部分,据此判断下列说法中正确的是( )


| A. | 钴元素的符号是CO | |
| B. | 铁元素的相对原子质量是55.85g | |
| C. | 从左到右各元素的原子序数依次增大 | |
| D. | 铬元素的原子核内有28个质子 |
5.下列有关化学知识的描述正确的是( )
| A. | 催化剂不仅能改变化学反应速率,而且会增加生成物的质量 | |
| B. | 电解水时正极产生氢气,负极产生氧气,其体积比为2:1 | |
| C. | 氢氧化钠固体易潮解,溶于水时放热 | |
| D. | 塑料给环境带来了污染,因此要全面禁止生产和使用 |
12.结合如表给出的KNO3、NaCl两种固体物质的溶解度,回答有关问题:
(1)20℃时,将40gKNO3放在100g水中充分溶解,所得溶液的质量是131.6g;
(2)这两种物质中,溶解度受温度变化影响较小的是氯化钠;
(3)将90gKNO3和30gNaCl组成的混合物放入100g60℃的水中充分搅拌,当温度降低到20℃时,发现有较多固体析出,下列有关说法中,正确的是AB.
A、60℃时固体全部溶解
B、析出的固体全部是KNO3
C、剩余溶液中只有NaCl.
| 0 | 20 | 40 | 60 | 80 | 100 | |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)这两种物质中,溶解度受温度变化影响较小的是氯化钠;
(3)将90gKNO3和30gNaCl组成的混合物放入100g60℃的水中充分搅拌,当温度降低到20℃时,发现有较多固体析出,下列有关说法中,正确的是AB.
A、60℃时固体全部溶解
B、析出的固体全部是KNO3
C、剩余溶液中只有NaCl.
10.除去下列各物质中混有的少量杂质,所用试剂、方法正确的是( )
| 序号 | 物质 | 杂质 | 试剂、方法 |
| A | CO2 | CO | 点燃 |
| B | NaOH溶液 | Na2CO3溶液 | 适量的稀盐酸 |
| C | MgCl2溶液 | 盐酸 | 适量的氢氧化钠溶液 |
| D] | FeSO4溶液 | CuSO4 | 过量铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
 化学与资源
化学与资源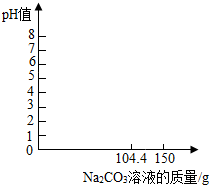 某兴趣小组需要配制100g质量分数为9.8%的稀硫酸,假设常温下该稀硫酸的pH值为0.在装有100g该稀硫酸的烧杯中加入104.4gNa2CO3溶液,恰好完全反应,溶液呈中性.
某兴趣小组需要配制100g质量分数为9.8%的稀硫酸,假设常温下该稀硫酸的pH值为0.在装有100g该稀硫酸的烧杯中加入104.4gNa2CO3溶液,恰好完全反应,溶液呈中性.