题目内容
工业上用煅烧石灰石的方法生产石灰,(CaO)同时得到产物(CO2),求50t含杂质为百分之十的石灰石能生产多少生石灰?并且能得到多少CO2.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据化学方程式,已知碳酸钙质量可求出氧化钙的质量以及二氧化碳的质量.
解答:解:设生成CaO的质量为x
50t含杂质为百分之十的石灰石的碳酸钙的质量=50t×(1-10%)=45t
CaCO3
CaO+CO2↑
100 56
45t x
=
x=25.2t
由质量守恒定律可知,生成二氧化碳的质量=45t-25.2t=19.8t
答:可得到氧化钙的质量为25.2t,同时得到二氧化碳的质量为19.8t.
50t含杂质为百分之十的石灰石的碳酸钙的质量=50t×(1-10%)=45t
CaCO3
| ||
100 56
45t x
| 100 |
| 45t |
| 56 |
| x |
x=25.2t
由质量守恒定律可知,生成二氧化碳的质量=45t-25.2t=19.8t
答:可得到氧化钙的质量为25.2t,同时得到二氧化碳的质量为19.8t.
点评:本题考查了化学方程式的简单计算,属于基础知识考查.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
物质名称正确的是( )
| A、HNO3:硝酸氢 |
| B、NO2:二氧化氮 |
| C、Fe(OH)2:氢氧化铁 |
| D、CuSO4:胆矾 |
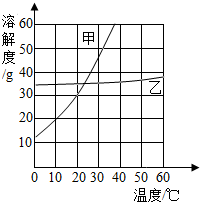 水、能源和环境与人类的生活和社会发展密切相关,回答下列问题.
水、能源和环境与人类的生活和社会发展密切相关,回答下列问题.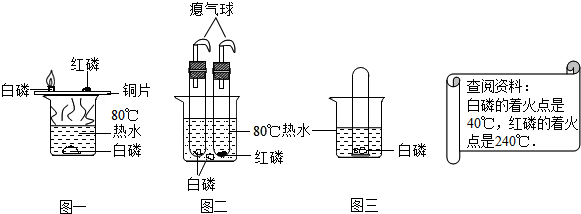
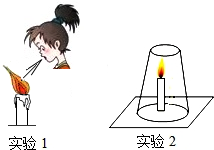
 如图是某品牌补铁剂的标签.请回答:
如图是某品牌补铁剂的标签.请回答:
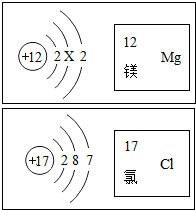 如图是镁和氯两种元素的有关信息,请回答下列问题:
如图是镁和氯两种元素的有关信息,请回答下列问题: