题目内容
4.已知电子的质量约为质子(或中子)质量的1/1836,下表是几种原子的构成和它们的相对原子质量.| 原子种类 | 原子核 | 核外电子数 | 相对原子质量 | |
| 质子数 | 中子数 | |||
| 氢(H) | 1 | 0 | 1 | 1 |
| 氦(He) | 2 | 2 | 2 | 4 |
| 氮(N) | 7 | 7 | 7 | 14 |
| 氧(O) | 8 | 8 | 8 | 16 |
| 铁(Fe) | 26 | 30 | 26 | 56 |
| 铀235(U235) | 92 | 143 | 92 | 235 |
①有些原子可以没有中子;
②相对原子质量≈质子数+中子数;
③不同种类的原子质子数不同.
分析 可以根据构成原子的微粒之间的数量关系及其相对原子质量方面的内容进行分析、判断,从而得出正确的结论;在原子中,核电荷数=核内质子数=核外电子数=原子序数.原子中一定含有质子、电子,中子是否含有要看是哪种原子,例如普通氢原子中不含中子,相对原子质量等于质子数与中子数之和.
解答 解:根据题中数据可总结出以下规律:原子核内不一定有中子;相对原子质量≈质子数+中子数;不同种类的原子质子数不同;原子核内质子数不一定等于中子数.
故答案为:①有些原子可以没有中子; ②相对原子质量≈质子数+中子数;③不同种类的原子质子数不同.
点评 本题主要考查了原子中各种微观粒子的数量关系问题,难度不大.

练习册系列答案
相关题目
15.下列说法错误的是( )
| A. | 二氧化碳气体能使澄清石灰水变浑浊 | |
| B. | 氮气一般不能燃烧,也不能支持燃烧 | |
| C. | 空气是由氧气和氮气组成的物质 | |
| D. | 稀有气体是氦、氖、氩、氪、氙等气体的总称 |
9.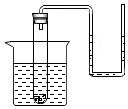 把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )
把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )
 把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )
把盛有饱和硝酸钾溶液(内含少量未溶解的KNO3晶体)的试管与一根U形管连通,U形管内盛有水,并将试管插在盛水的烧杯中(如图所示).如果往烧杯中缓慢加入硝酸铵晶体,此时试管内的KNO3溶液的质量以及U形管中液面变化分别是( )| A. | 减少、左高右低 | B. | 增加、左高右低 | C. | 减少、左低右高 | D. | 增加、左低右高 |
