题目内容
2.质量守恒定律的发现对化学的发展做出了重要贡献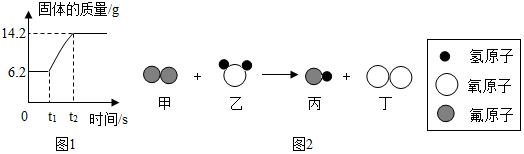
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是BC(填标号)
A、蔗糖和水 B、碳酸钠和稀盐酸 C、铁和硫酸铜溶液
(2)在氧气中点燃红磷的实验过程,固体质量变化如图1所示:
①从燃烧条件分析,固体质量在t1前没有发生变化的原因是温度未达到红磷的着火点.
②该反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)某反应的微观示意图如图2所示:
①该反应中属于单质的物质是氟气、氧气;
②参加反应的甲物质和生成的丙物质分子数目比为1:2.
分析 (1)根据已有的知识进行分析解答,质量守恒定律是化学变化中物质质量的守恒,据此解答;
(2)根据质量守恒定律及其应用回答,将一定质量的红磷在一瓶氧气中充分燃烧,反应后生成五氧化二磷.
(3)观察微观示意图,根据微粒的构成分析物质的类别及名称,分析反应物、生成物,写出反应的化学方程式.
解答 解:(1)A、蔗糖和水是溶解过程,是物理变化,不能直接用于验证质量守恒定律;
B、碳酸钠和稀盐酸反应生成二氧化碳气体,属于化学变化,在密闭容器中能直接用于验证质量守恒定律;
C、铁和硫酸铜溶液,铁比铜活泼,可以将铜置换出来,是化学变化,能直接用于验证质量守恒定律;
故选BC.
(2)①从燃烧条件分析,固体质量在t1前没有发生变化的原因为温度未达到红磷的着火点;
②红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(3)由物质的微观构成可知,该反应的化学方程式为:2F2+2H2O=4HF+O2;
①该反应氟气、氧气都属于单质;
②参加反应的甲物质和生成的丙物质分子数目比为2:4=1:2.
故答案为:
(1)BC;(2)①温度未达到红磷的着火点;②4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;(3)①氟气、氧气;②1:2.
点评 本题考查的是质量守恒定律的验证,完成此题的关键是抓住化学变化.运用质量守恒定律时,一定不能漏掉反应物或生成物的质量,特别是气体物质的质量.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
12.10℃时,50克水里最多溶解甲物质10克,20℃时100克水里最多溶解乙物质20克,则甲、乙两物质的溶解度的关系为( )
| A. | 甲>乙 | B. | 甲=乙 | C. | 甲<乙 | D. | 无法确定 |
3.下列物质的俗称与化学式不相符合的是( )
| A. | 干冰 CO2 | B. | 生石灰 Ca(OH)2 | C. | 烧碱 NaOH | D. | 食盐NaCl |
4. 碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )
碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )
 碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )
碳和部分碳的化合物间转化关系如图所示.下列说法中错误的是( )| A. | 固态X俗名叫“干冰”,常用作制冷剂 | |
| B. | H2CO3能紫色石蕊溶液变成红色,说明X具有酸性 | |
| C. | 反应2CuO+C $\frac{\underline{\;高温\;}}{\;}$ 2Cu+X↑体现了碳的还原性 | |
| D. | X转化为CO的反应为X+C$\frac{\underline{\;高温\;}}{\;}$2CO |