题目内容
5.硝酸银在光照条件下分解.除生成NO2气体外,还生成两种单质.请写出该反应的化学方程式:2AgNO3$\frac{\underline{\;光照\;}}{\;}$2Ag+2NO2↑+O2↑,该反应中有三种元素的化合价发生了变化.分析 由质量守恒定律可知,硝酸银在光照条件下分解.除生成NO2气体外,还生成两种单质应该是银和氧气,写出反应的化学方程式即可,然后根据常见元素的化合价进行解答;
解答 解:硝酸银见光分解生成NO2、金属银、氧气,反应的化学方程式为2AgNO3$\frac{\underline{\;光照\;}}{\;}$2Ag+2NO2↑+O2↑;反应前,银元素显+1价,氮元素显+5价,氧元素显-2价,反应后单质中元素的化合价为0,故银元素为0价,氧元素为0价,氮元素为+4价,故三种元素的化合价发生了变化;
故答案为:2AgNO3$\frac{\underline{\;光照\;}}{\;}$2Ag+2NO2↑+O2↑;三;
点评 本题难度不大,掌握化学方程式的书写方法、常见元素的化合价是正确解答本题的关键.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
16.下列符号中,既有宏观意义,又有微观意义的是( )
| A. | Mg2+ | B. | Zn | C. | Al3+ | D. | 2Cu |
20.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用10g石灰石样品,把40g稀盐酸分4次加入样品中(样品中除碳酸钙外,杂质既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
(1)a=2
(2)该石灰水样品中碳酸钙的质量分数是80%;
(3)前两次一共生成的二氧化碳气体质量多少克?(写出计算过程)
| 稀盐酸的用量 | 第一次加入10g | 第二次加入10g | 第三次加入10g | 第四次加入10g |
| 剩余固体的质量 | 7g | 4g | 2g | ag |
(2)该石灰水样品中碳酸钙的质量分数是80%;
(3)前两次一共生成的二氧化碳气体质量多少克?(写出计算过程)
9.下列物质在氧气中燃烧能够产生蓝紫色火焰的是( )
| A. | 磷 | B. | 碳 | C. | 铁 | D. | 硫 |
10.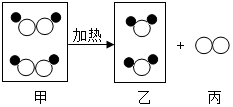 如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )
如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )
 如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )
如图是某反应的微观示意图,若○表示氧原子,●表示氢原子,有关说法正确的是( )| A. | 该反应属于分解反应 | |
| B. | 该反应前后分子种类没有改变 | |
| C. | 该反应前后原子种类改变 | |
| D. | 图中甲、乙两种物质是由分子构成,丙物质由原子构成 |
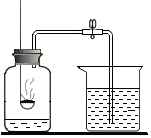 用如图所示的实验装置来测定空气里氧气的含量,请回答下列问题
用如图所示的实验装置来测定空气里氧气的含量,请回答下列问题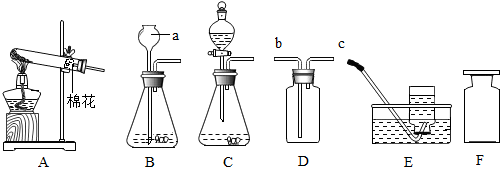
 根据相应问题回答下列问题.
根据相应问题回答下列问题.