题目内容
17.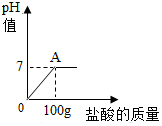 在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示
在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示(1)100g稀盐酸中氯化氢的质量7.3g.
(2)完全反应后,所得溶液中溶质的质量分数?
分析 题目给出了消耗的稀盐酸的质量以及质量分数,所以根据HCl的质量和对应的化学方程式求算碳酸钠和氯化钠、二氧化碳的质量,进而求算对应的质量分数.
解答 解:
100g质量分数为7.3%稀盐酸含有的HCl的质量为100g×7.3%=7.3g
设碳酸钠的质量为x,生成氯化钠的质量为y,生成二氧化碳的质量为z.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x 7.3g y z
$\frac{106}{x}$=$\frac{73}{7.3g}$=$\frac{117}{y}$=$\frac{44}{z}$
x=10.6g
y=11.7g
z=4.4g
完全反应后,所得溶液中溶质的质量分数为$\frac{13.6g-10.6g+11.7g}{13.6g+100g-4.4g}$×100%≈13.5%
答:(1)100g稀盐酸中氯化氢的质量 7.3g.
(2)完全反应后,所得氯化钠溶液中溶质的质量分数为13.5%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
15.西瓜中的化学
夏季,香甜可口、营养丰富的西瓜是人们喜爱的水果之一,下表列出的是每100g某品种西瓜可食用部分的主要营养成分数据.
(1)表中“X“是一种人体必须的营养素,它是维生素,其对人体的主要作用是调节新陈代、预防疾病.营养成分中含的Fe、Zn.(填元素符号)属于人体必需的微量元素.
(2)西瓜的“甜”是因其含有葡萄糖、蔗糖等糖类,它是西瓜光合作用的产物,试写出西瓜通过光合作用产生葡萄糖的化学反应方程式6CO2+6H2O$\frac{\underline{\;光照\;}}{\;}$C6H12O6+6O2.
(3)有人说,食用西瓜不能为人体补充能量.据西瓜的成分分析该说法是否正确,为什么?不正确;西瓜中含有的蛋白质、脂肪和糖类都可提供能量.
(4)西瓜种植过程中需施用化肥增加产量,下列属于复合肥的是CD(填字母).
A.NH4HCO3 B.Ca(H2PO4)2 C.NH4H2PO4 D.KNO3.
夏季,香甜可口、营养丰富的西瓜是人们喜爱的水果之一,下表列出的是每100g某品种西瓜可食用部分的主要营养成分数据.
| 营养成分 | 水分 | 蛋白质 | 脂肪 | 糖类 | X | 钙、磷、铁、锌 |
| 质量 | 92.5g | 0.7g | 0.2g | 6.1g | 6.8mg | 17.1mg |
(2)西瓜的“甜”是因其含有葡萄糖、蔗糖等糖类,它是西瓜光合作用的产物,试写出西瓜通过光合作用产生葡萄糖的化学反应方程式6CO2+6H2O$\frac{\underline{\;光照\;}}{\;}$C6H12O6+6O2.
(3)有人说,食用西瓜不能为人体补充能量.据西瓜的成分分析该说法是否正确,为什么?不正确;西瓜中含有的蛋白质、脂肪和糖类都可提供能量.
(4)西瓜种植过程中需施用化肥增加产量,下列属于复合肥的是CD(填字母).
A.NH4HCO3 B.Ca(H2PO4)2 C.NH4H2PO4 D.KNO3.
16.下列不属于合金的是( )
| A. | 焊锡 | B. | 黄铜 | C. | 石墨 | D. | 生铁 |
12.下列说法正确的是( )
| A. | 所有含碳元素的化合物都是有机物 | |
| B. | 草木灰的主要成分是碳酸钾、碳酸钾属于复合肥料 | |
| C. | 做饭时,若燃气灶的火焰呈现黄色,锅底出现黑色,则需要调大灶具的进风口 | |
| D. | 一氧化碳有毒,燃着的煤炉会产生一氧化碳,在煤炉上放一壶水能防止人中毒 |
2.化学与生活息息相关,下列说法有科学性错误的是( )
| A. | 久未开启的地窖、枯井等地方CO2含量高,冒然进入易窒息 | |
| B. | 在化粪池等有沼气的井盖口燃放鞭炮,易引起爆炸 | |
| C. | 透视检测肠胃疾病时口服硫酸钡,不会对人体造成危害 | |
| D. | 用煤炉取暖时,在屋里洒些石灰水可防CO中毒 |
6.掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一.
根据物质在转化过程中的特点,可将化学反应分为化合反应、分解反应、置换反应和复分解反应四种基本反应类型.下列转化不属于这四种基本反应类型的是B.
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一种重要途径.实验室中可用KMnO4受热分解制取氧气,并将反应后的混合物进行分离回收.实验操作如图所示(MnO2难溶于水):
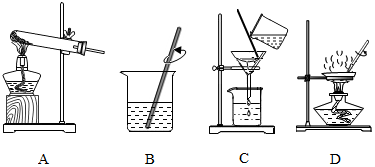
写出A中发生反应的方程式2KMnO4=K2MnO4+MnO2+O2↑;
图B操作中玻璃棒的作用是搅拌加速溶解.
②操作中的一处明显错误是漏斗的下端管口没有紧靠烧杯内壁;图D操作中,当看到蒸发皿中有较多量固体析出时,停止加热.
(3)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论.
①下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB═cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如下表:
则x=88;有机化合物R中碳元素的质量分数为52.2%.
(1)分类是学习化学的重要方法之一.
根据物质在转化过程中的特点,可将化学反应分为化合反应、分解反应、置换反应和复分解反应四种基本反应类型.下列转化不属于这四种基本反应类型的是B.
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一种重要途径.实验室中可用KMnO4受热分解制取氧气,并将反应后的混合物进行分离回收.实验操作如图所示(MnO2难溶于水):

写出A中发生反应的方程式2KMnO4=K2MnO4+MnO2+O2↑;
图B操作中玻璃棒的作用是搅拌加速溶解.
②操作中的一处明显错误是漏斗的下端管口没有紧靠烧杯内壁;图D操作中,当看到蒸发皿中有较多量固体析出时,停止加热.
(3)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论.
①下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB═cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物质的质量如下表:
| R | O2 | CO2 | H2O | |
| 反应前质量/g | 46 | 128 | 0 | 0 |
| 反应后质量/g | 0 | 32 | x | 54 |
7.金属材料在工农业生产、日常生活中广泛应用,下列说法错误的是( )
| A. | 铁制品锈蚀的过程实际上是铁与氧气发生的化学反应 | |
| B. | 铝制品不易锈蚀的原因是铝与氧气作用在表面形成致密薄膜 | |
| C. | 电池中含有铅、镍、镉、汞等金属,随意丢弃电池会造成污染 | |
| D. | 合金的很多性能与组成它们的纯金属不同,合金具有更广泛的用途 |
