题目内容
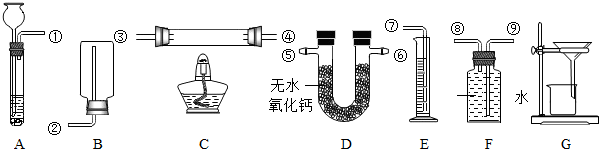
某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质.结合装置图,回答下列问题:
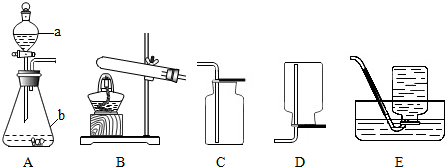
(1)写出图中标号仪器的名称:a ,b .
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是 (填上图字母),可选用C装置收集氧气,其原因是 .
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是 (填上图字母).
(4)实验室制取二氧化碳的化学方程式是 ;若要证明二氧化碳能与水发生反应,应向烧杯的水中加入 .

(1)写出图中标号仪器的名称:a
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是
(4)实验室制取二氧化碳的化学方程式是
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟记常用仪器的名称即可轻松作答.
(2)根据利用过氧化氢在二氧化锰催化下制取氧气时所使用药品的状态与反应条件,确定此时所应选用的发生装置,根据氧气的物理性质决定其收集方法;
(3)发生装置主要由反应物的状态和反应条件决定;
(4)根据实验室制取二氧化碳反应原理解答,证明二氧化碳能与水发生反应在水中加入石蕊试液.
(2)根据利用过氧化氢在二氧化锰催化下制取氧气时所使用药品的状态与反应条件,确定此时所应选用的发生装置,根据氧气的物理性质决定其收集方法;
(3)发生装置主要由反应物的状态和反应条件决定;
(4)根据实验室制取二氧化碳反应原理解答,证明二氧化碳能与水发生反应在水中加入石蕊试液.
解答:解::(1)a为分液漏斗,b为锥形瓶;
(2)用过氧化氢溶液与二氧化锰混合制取氧气,所选择用药品为固体与液体反应且不需要加热,因此应选用发生装置B作为制取氧气的发生装置;在二氧化锰催化下过氧化氢分解生成水和氧气,氧气密度比空气大故可以选择C装置收集氧气;
(3)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;
(4)实验室制取二氧化碳用的是稀盐酸和石灰石,化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,证明二氧化碳能与水发生反应在水中加入石蕊试液.因为二氧化碳遇水生成的碳酸显酸性能使石蕊试液变红色;
答案:(1)分液漏斗 锥形瓶;
(2)A 氧气的密度比空气大;
(3)B;
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑,石蕊试液.
(2)用过氧化氢溶液与二氧化锰混合制取氧气,所选择用药品为固体与液体反应且不需要加热,因此应选用发生装置B作为制取氧气的发生装置;在二氧化锰催化下过氧化氢分解生成水和氧气,氧气密度比空气大故可以选择C装置收集氧气;
(3)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;
(4)实验室制取二氧化碳用的是稀盐酸和石灰石,化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,证明二氧化碳能与水发生反应在水中加入石蕊试液.因为二氧化碳遇水生成的碳酸显酸性能使石蕊试液变红色;
答案:(1)分液漏斗 锥形瓶;
(2)A 氧气的密度比空气大;
(3)B;
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑,石蕊试液.
点评:本道题主要考查了实验室制取气体发生装置和收集装置的选取,发生装置主要由反应物的状态和反应条件决定,收集装置主要由气体的密度和溶水性决定,另外还要考虑气体是否与水反应、是否与空气反应、是否有毒等等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、森林火灾时,用炸弹轰炸灭火,利用了“隔离可燃物”原理 |
| B、带火星的木条一定能在含有氧气的集气瓶中复燃 |
| C、酸能够使紫色石蕊溶液变红,二氧化碳能使紫色石蕊溶液变红色,所以二氧化碳是酸 |
| D、将酚酞试液滴入某溶液中,通过酚酞颜色的变化判断该溶液是否属于碱 |
下列实验操作或事故处理正确的是( )
| A、制取Fe(OH)2时,将装有NaOH溶液的滴管插入盛有FeSO4溶液的试管中 |
| B、实验结束后,为节约时间,可用嘴吹灭酒精灯 |
| C、皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗,再用大量水冲洗 |
| D、稀释浓硫酸时,将水沿器壁慢慢注入浓硫酸中,并不断搅拌 |
下列方法能直接从海水制取可饮用水的是( )
| A、萃取 | B、结晶 | C、蒸馏 | D、过滤 |