题目内容
3.石灰石的主要成分为碳酸钙,含钙36%的石灰石的纯度为( )| A. | 29% | B. | 95% | C. | 90% | D. | 80% |
分析 根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%计算碳酸钙的质量.
解答 解:设该石灰石的质量为100g,则含钙36g.
所以碳酸钙的质量是:$\frac{36g}{\frac{40}{100}×100%}$=90g,
所以含钙36%的石灰石的纯度为:$\frac{90g}{100g}$×100%=90%.
故选:C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
14.水是生命之源,下列有关水的说法正确的是( )
| A. | 将河水经过沉淀、过滤、活性炭吸附等净化处理后,所得的水就是纯水 | |
| B. | 水是一种常见的溶液 | |
| C. | 煮沸可以降低自来水的硬度 | |
| D. | 电解水实验说明水是由氢气和氧气组成的 |
18.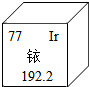 南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
 南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )| A. | 铱的原子序数为115 | B. | 铱原子的核电荷数为77 | ||
| C. | 铱的相对原子质量为192.2g | D. | 铱原子的核内中子数为80 |
15.下列化学用语书写正确的是( )
| A. | 氧化铝AL3O2 | B. | 氯化钙Cacl | C. | 铵根离子NH4+ | D. | 高锰酸钾K2MNO4 |
13.氢化钙(CaH2)可作为生氢剂,反应的化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑,下列说法不正确的是( )
| A. | CaH2 既是还原剂,又是氧化剂 | B. | H2 既是氧化产物,又是还原产物 | ||
| C. | CaH2 是还原剂,H2O 是氧化剂 | D. | 氧化产物与还原产物质量比为1:1 |

 ,该图表示(填序号)C.
,该图表示(填序号)C.
 海水是一种化学成分复杂的混合物,除了水还包括溶解于水中的丰富的矿物质和少量气体.以海水为原料可以生产许多化工产品:如氯化钠、氢氧化钠、氢气、氯气、镁、食用加碘盐等.
海水是一种化学成分复杂的混合物,除了水还包括溶解于水中的丰富的矿物质和少量气体.以海水为原料可以生产许多化工产品:如氯化钠、氢氧化钠、氢气、氯气、镁、食用加碘盐等.