题目内容
某自然科学兴趣小组,用不同金属跟稀硫酸反应来研究反应的快慢,他们选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积,相同质量分数的稀硫酸反应,观察30秒内从导管口冒出的氢气泡多少.(“+”越多表示产生的气泡越多).
如果四种金属分别是镁、铝、铁、锌中的一种,则丁最有可能是( )
| 金属 | 甲 | 乙 | 丙 | 丁 |
| 氢气气泡多少 | ++ | ++++ | +++ | + |
| A、镁 | B、铝 | C、铁 | D、锌 |
考点:金属的化学性质
专题:金属与金属材料
分析:本题研究不同金属跟稀硫酸反应的快慢,利用表格中的记录可判断气泡的多少来得出金属的活泼性强弱.
解答:解:因取用大小相同的金属片,相同体积、相同质量分数的稀硫酸,时间相同,则气泡的多少可说明反应进行的快慢,根据表格中的记录可知:金属的活泼性为乙>丙>甲>丁,而镁、铝、铁、锌的活泼性为镁>铝>锌>铁,则丁最有可能是铁.
故选C.
故选C.
点评:本题以实验探究的方式利用金属与酸的反应的实验记录来考查金属活泼性,学生应能利用表格中的记录作出正确的判断.

练习册系列答案
相关题目
 去年10月,石墨烯的制备者获得了诺贝尔奖.石墨烯是从石墨材料中剥离出来的单层固体单质(结构如图),它不仅是已知材料中最薄的一种,还非常牢固坚硬.关于石墨烯的说法中错误的是( )
去年10月,石墨烯的制备者获得了诺贝尔奖.石墨烯是从石墨材料中剥离出来的单层固体单质(结构如图),它不仅是已知材料中最薄的一种,还非常牢固坚硬.关于石墨烯的说法中错误的是( )| A、石墨烯与C60是同一种物质 |
| B、石墨烯是一种单质 |
| C、石墨烯的硬度很大 |
| D、石墨烯完全燃烧后的产物是CO2 |
下列物质能导电的是( )
| A、蒸馏水 | B、蔗糖溶液 |
| C、食盐水 | D、液氧 |
通过下列化学反应不能达到目的是( )
| A、用铁和氯化铜溶液制氯化铁:2Fe+3CuCl2=2FeCl3+3Cu | ||||
| B、用稀硫酸除去炭粉中的少量氧化铜:CuO+H2SO4═CuSO4+H2O | ||||
| C、证明金属锰(Mn)比铜活泼:Mn+CuSO4═MnSO4+Cu | ||||
D、用氧化铜去除CO2中的CO:CuO+CO
|
甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如表所示:下列判断正确的是( )
| 物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
| A、表中a的值为2.6 |
| B、X一定是该反应的催化剂 |
| C、X可能含有氢元素 |
| D、若增加氧气量,则生成物的种类可能减少 |
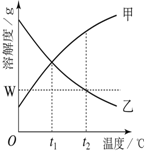 如图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入w g甲 和w g乙(两种物质溶解时互不影响),充分搅拌.将混合物的温度降低到t1℃.下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线.在t2℃时向盛有100g水的烧杯中先后加入w g甲 和w g乙(两种物质溶解时互不影响),充分搅拌.将混合物的温度降低到t1℃.下列说法正确的是( )| A、甲物质的溶解度随温度升高而减小 |
| B、温度降低到t1℃时,得到甲、乙的饱和溶液 |
| C、温度降低到t1℃时,得到甲、乙的不饱和溶液且甲、乙的溶质质量分数相等 |
| D、t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液 |
 如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算: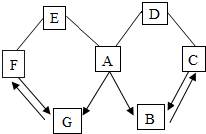 如图所示 A~G 是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知 B 是光合作用的原料,G 是最清洁的能源,且 B、C、D、E、F 都是氧化物.请回答:
如图所示 A~G 是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知 B 是光合作用的原料,G 是最清洁的能源,且 B、C、D、E、F 都是氧化物.请回答: