题目内容
7.已知双氧水制氧气,向锥形瓶中加入20g双氧水和1g二氧化锰,反应后锥形瓶中剩余物质的质量为19.4g①反应后二氧化锰的质量为多少?
②生成氧气的质量为多少?
③双氧水的质量分数为多少?
分析 ①二氧化锰作催化剂,反应前后质量不变;
②反应前后锥形瓶中物质的质量差即为生成氧气的质量;
③根据氧气的质量可以计算过氧化氢的质量,进一步可以计算过氧化氢溶液中溶质的质量分数.
解答 解:①反应结束后,过滤,滤渣是二氧化锰,因为二氧化锰是催化剂,反应前后质量不变,所以滤渣的质量是1.0g.
故填:1.0.
②生成氧气的质量为:20.0g+1.0g-20.2g=0.8g.
故填:0.8.
③设过氧化氢的质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x 0.8g
$\frac{68}{x}=\frac{32}{0.8g}$
x=1.7g,
过氧化氢溶液中溶质的质量分数为:$\frac{1.7g}{20g}$×100%=8.5%;
答案:
①反应后二氧化锰的质量为1g;
②生成氧气的质量为0.8g;
③过氧化氢溶液中溶质的质量分数为8.5%.
点评 差量法在计算中经常遇到,要掌握差量法计算的技巧,并且能够熟练运用,对解答计算方面的题目帮助很大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
17.过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液80克分4次加入到同一个盛有适量二氧化锰的烧杯中,待充分反应,溶液不再产生气泡后称量得到如下数据
(1)小军认为表中的m不需再测了,它的值为101.6.
(2)计算该瓶过氧化氢溶液中溶质的质量分数.
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入过氧化氢溶液的质量(克) | 20 | 20 | 20 | 20 |
| 烧杯和烧杯中物质的总质量(克) | 46.4 | 64.8 | 83.2 | m |
(2)计算该瓶过氧化氢溶液中溶质的质量分数.
15.逻辑推理是化学学习中常用的思维方法.下列推理结果正确的是( )
| A. | 燃烧伴有发光放热现象,所以有发光放热现象就一定是燃烧 | |
| B. | KNO3溶于水时溶液温度无明显变化,则NH4NO3溶于水时溶液温度也无明显变化 | |
| C. | 化合物都是由不同种元素组成的,所以不同种元素组成的纯净物一定是化合物 | |
| D. | 二氧化碳是由分子构成的气体,所以所有的气体都是由分子构成的 |
2.对饱和熟石灰溶液进行如下操作,其中不会看到晶体析出的是( )
| A. | 加入一定量NaOH | B. | 加入一定量的NH4NO3 | ||
| C. | 加热 | D. | 恒温蒸发一定量溶剂 |
12.下列选项属于可再生资源的是( )
| A. | 石油 | B. | 煤炭 | C. | 天然气 | D. | 沼气 |
16.下列做法有利于减少空气中固体颗粒物的是( )
| A. | 大力发展火电 | B. | 露天焚烧秸秆 | C. | 开发清洁能源 | D. | 提倡多开汽车 |
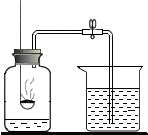 如图所示,在集气瓶中加入少量水,并做上记号.用弹簧夹夹紧胶管,点燃燃烧匙内过量的红磷后.立即伸人瓶中并把塞子塞紧.观察红磷燃烧的现象.待红磷熄灭并冷却后.打开弹簧夹.观察实验现象.
如图所示,在集气瓶中加入少量水,并做上记号.用弹簧夹夹紧胶管,点燃燃烧匙内过量的红磷后.立即伸人瓶中并把塞子塞紧.观察红磷燃烧的现象.待红磷熄灭并冷却后.打开弹簧夹.观察实验现象.