题目内容
3.用化学用语表示2个铁离子2Fe3+、硫酸根离子SO42-、氦气He、硝酸铝中铝元素的化合价$\stackrel{+3}{Al}$(NO3)3、酒精燃烧的化学方程式C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
分析 离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
氦气属于稀有气体单质,直接用元素符号表示其化学式.
化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
酒精燃烧生成二氧化碳和水,写出反应的化学方程式即可.
解答 解:离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.2个铁离子、硫酸根离子分别可表示为:2Fe3+、SO42-.
氦气属于稀有气体单质,直接用元素符号表示其化学式,其化学式为He.
硝酸铝中硝酸根显-1价,铝元素显+3价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硝酸铝中铝元素的化合价可表示为:$\stackrel{+3}{Al}$(NO3)3.
酒精燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答案为:2Fe3+;SO42-;He;$\stackrel{+3}{Al}$(NO3)3;C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
点评 本题难度不大,掌握常见化学用语(化学式、化合价、离子符号、化学方程式等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
1.下列实验现象的描述不正确的是( )
| A. | 红磷燃烧产生大量白烟 | |
| B. | 铜丝与硝酸银溶液反应,溶液有无色变成蓝色 | |
| C. | 木炭和氧化铜在高温下反应会有红色物质生成 | |
| D. | 硫在氧气中燃烧产生淡蓝色火焰 |
14.根据下列四种粒子的结构示意图,所获取的信息正确的是( )


| A. | 它们表示四种元素的原子 | |
| B. | ①③④表示的是阳离子 | |
| C. | ④表示的元素是非金属元素 | |
| D. | ②表示的元素在化合物中通常显+2价 |
11.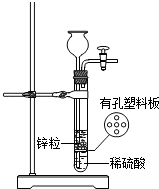 小新在实验室用足量的锌粉与稀硫酸按图装置制取一定量的氢气,发现液面刚好不与锌粒接触而又无酸液可加,若从长颈漏斗中加入适量下列试剂,又不影响生成氢气的量,你认为最合适的是( )
小新在实验室用足量的锌粉与稀硫酸按图装置制取一定量的氢气,发现液面刚好不与锌粒接触而又无酸液可加,若从长颈漏斗中加入适量下列试剂,又不影响生成氢气的量,你认为最合适的是( )
 小新在实验室用足量的锌粉与稀硫酸按图装置制取一定量的氢气,发现液面刚好不与锌粒接触而又无酸液可加,若从长颈漏斗中加入适量下列试剂,又不影响生成氢气的量,你认为最合适的是( )
小新在实验室用足量的锌粉与稀硫酸按图装置制取一定量的氢气,发现液面刚好不与锌粒接触而又无酸液可加,若从长颈漏斗中加入适量下列试剂,又不影响生成氢气的量,你认为最合适的是( )| A. | 氢氧化钠溶液 | B. | 碳酸钠溶液 | C. | 硫酸钠溶液 | D. | 澄清石灰水 |
18.下列说法正确的是( )
| A. | 混合物一定由不同种分子构成 | B. | 化合物中一定含有不同种元素 | ||
| C. | 只含有一种元素的物质一定是单质 | D. | 含有氧元素的物质一定是氧化物 |
8.氧化钙和氢氧化钠固体混合物,俗称“碱石灰”.在实验室里常用作干燥剂.碱石灰在空气中久置会变质,某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示试验流程.
请你参与探究过程:
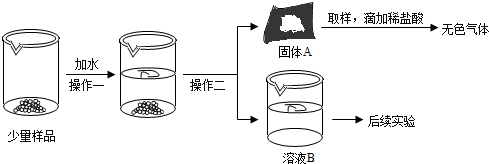
(1)在操作一实验过程中,同学们发现向样品中加水时还放出大量的热.据此实验,下列对样品成分分析正确的是D(填序号).
A.一定有氢氧化钠 B.一定有氢氧化钙 C.一定有氧化钙 D.至少有氧化钙、氢氧化钠中的一种
(2)为了使样品充分溶解,操作一中 还要用到的玻璃仪器是玻璃棒.
(3)固体A中一定含有碳酸钙(CaCO3).
(4)溶液B成分的探究.
【查阅资料】
①氢氧化钙、碳酸钠溶于水无明显的温度变化;
②氯化钙溶液呈中性
【猜想】
溶液B中溶质可能为:①氢氧化钠; ②碳酸钠; ③氢氧化钠和碳酸钠;④氢氧化钙和氢氧化钠
【设计方案并进行试验】
实验步骤①中发生的化学反应方程式是CaCl2+Na2CO3=2NaCl+CaCO3↓.
请你参与探究过程:

(1)在操作一实验过程中,同学们发现向样品中加水时还放出大量的热.据此实验,下列对样品成分分析正确的是D(填序号).
A.一定有氢氧化钠 B.一定有氢氧化钙 C.一定有氧化钙 D.至少有氧化钙、氢氧化钠中的一种
(2)为了使样品充分溶解,操作一中 还要用到的玻璃仪器是玻璃棒.
(3)固体A中一定含有碳酸钙(CaCO3).
(4)溶液B成分的探究.
【查阅资料】
①氢氧化钙、碳酸钠溶于水无明显的温度变化;
②氯化钙溶液呈中性
【猜想】
溶液B中溶质可能为:①氢氧化钠; ②碳酸钠; ③氢氧化钠和碳酸钠;④氢氧化钙和氢氧化钠
【设计方案并进行试验】
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤①取少量溶液B于试管中,加入足量CaCl2溶液 步骤②过滤,在滤液中滴加酚酞试液 | 现象①有白色沉淀生成 现象②溶液由无色变为红色 | 猜想③正确 |
12.下列实验不能达到目的是( )
| 实验内容 | 所用试剂或方法 |
| A.除去硫酸亚铁溶液中的硫酸铜 | 加入过量的铁粉,过滤 |
| B.鉴别氯化铵溶液和硝酸铵溶液 | 加入氢氧化钠溶液 |
| C.探究分子具有不停运动和分子之间有间隔的性质 | 加热固体碘 |
| D.探究燃烧条件:温度需要达到可燃物的着火点 | 在空气中隔着薄铜片同时加热滤纸块和乒乓球块 |
| A. | A | B. | B | C. | C | D. | D |
13.下列事实与金属活动性顺序无关的事( )
| A. | 银的导电性强于铜 | |
| B. | 不能与金属铜与稀硫酸反应制取氢气 | |
| C. | 铜能与硝酸银溶液反应置换出银 | |
| D. | 镁和铝分别与稀盐酸反应剧烈程度不同 |