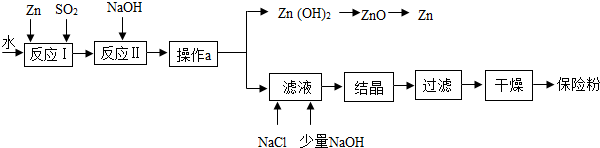
题目内容
4.实验室有一瓶长期暴露在空气中的氢氧化钠固体,某实验小组的同学对该产品的成分及含量进行了探究.【实验探究一】为得到纯净的氢氧化钠固体,并测定NaOH的纯度,小明设计的实验过程如图,请回答下列问题:
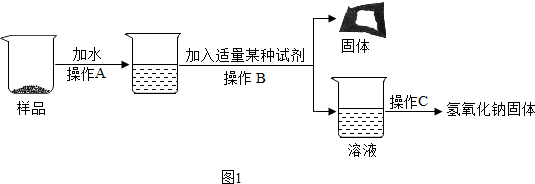
(1)长期暴露在空气中的氢氧化钠固体样品,其变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式作答).操作B中加入的试剂是Ca(OH)2(填写化学式).
(2)操作B的名称为过滤.
(3)若要测定该固体中NaOH的纯度,除上述过程中使用到的仪器外,还需补充的仪器是托盘天平.
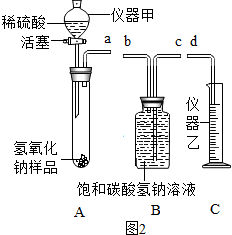
【实验探究二】为了测定NaOH的纯度,小红同学设计如图2装置(铁架台略去).
查询资料得知:
①碳酸氢钠溶液不吸收二氧化碳;
②中和反应均要放热.
(4)装置管口连接顺序为:a→b,c→d.
(5)仪器甲的名称是分液漏斗,使用该仪器有两个优点:一是可以控制稀硫酸的加入,二是节约药品.
(6)取10g样品进行实验,根据实验数据,通过计算可知产生了CO20.11g,则原样品中NaOH的纯度为93.75%.
【实验反思】
(7)有同学认为可以使用盐酸代替硫酸,你不同意(填“同意”或“不同意”)他的理由是盐酸具有挥发性.
分析 (1)根据氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氢氧化钙反应会生成碳酸钙沉淀和氢氧化钠进行分析;
(2)根据过滤可以将不溶性固体从溶液中分离出来进行分析;
(3)根据要测定该固体中NaOH的纯度,需要用托盘天平来称量样品和沉淀的质量进行分析;
(4)根据碳酸氢钠溶液不吸收二氧化碳,二氧化碳密度比液体密度小进行分析;
(5)根据实验室常用仪器的名称,以及长颈漏斗的作用进行分析;
(6)根据二氧化碳的质量和化学方程式进行计算;
(7)根据盐酸具有挥发性进行分析.
解答 解:(1)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2═Na2CO3+H2O,碳酸钠和氢氧化钙反应会生成碳酸钙沉淀和氢氧化钠,所以操作B中加入的试剂是Ca(OH)2;
(2)过滤可以将不溶性固体从溶液中分离出来,所以操作B的名称为:过滤;
(3)要测定该固体中NaOH的纯度,需要用托盘天平来称量样品和沉淀的质量,所以实验过程中一定还需用到的仪器是:托盘天平;
(4)碳酸氢钠溶液不吸收二氧化碳,二氧化碳密度比液体密度小,所以装置管口连接顺序为:a→b→c→d;
(5)通过分析题中所指仪器的作用可知,甲的名称是分液漏斗,使用该仪器有两个优点:一是可以控制稀硫酸的加入,二是节约药品;
(6)设碳酸钠的质量为x
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
x 0.11g
$\frac{106}{x}$=$\frac{44}{0.11g}$
x=0.265g
原样品中NaOH的纯度=$\frac{10g-0.265g}{10g}$×100%≈97.35%
答:原样品中NaOH的纯度是97.35%;
(7)盐酸具有挥发性,所以不能用盐酸代替硫酸.
故答案为:(1)2NaOH+CO2═Na2CO3+H2O,Ca(OH)2;
(2)过滤;
(3)托盘天平;
(4)b,c;
(5)分液漏斗,是节约药品;
(6)原样品中NaOH的纯度是97.35%;
(7)不同意,盐酸具有挥发性.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 阶梯计算系列答案
阶梯计算系列答案| A. | H2SO4 | B. | AgNO3 | C. | FeSO4 | D. | MgSO4 |
【查阅资料】:①CuCl2溶液、CuSO4溶液都呈蓝色,Cu(OH)2蓝色沉淀.
②CuSO4+BaCl2═BaSO4↓+CuCl2,BaSO4白色沉淀,不溶于水和盐酸.
【提出问题】:滤液中的溶质是什么物质?
【猜想假设】:甲同学认为:只含有CuCl2;
乙同学认为:一定含有CuCl2,可能含有CuSO4;
丙同学认为:一定含有CuCl2,肯能含有CuSO4和BaCl2
你认为:一定含有CuCl2,可能含有BaCl2.
【分析讨论】:丁同学认为丙同学的猜想肯定是不合理的,理由是CuSO4和BaCl2会继续发生反应.
【实验设计】:请你设计一个简单的实验来验证的猜想是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| 取滤液于试管中,逐渐滴加稀硫酸 | 产生白色沉淀 | 猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取滤液于试管中滴加少量的氢氧化钠溶液 | 产生蓝色沉淀 | 猜想正确 |
【反思拓展】:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑反应物是否完全反应.

(1)贝壳高温锻烧时,发生反应的化学方程式是CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(2)操作I的名称是过滤;
(3)该流程中没有涉及的基本反应类型是置换反应,;
(4)固体B的化学式为CaCO3;
【问题与发现】该小组同学所得固体C一定是纯净的NaOH吗?
【猜想与假设】根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH 乙:NaOH和Na2CO3的混合物 丙:NaOH和Ca(OH)2的混合物
【探究与验证】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.实验操作、现象和结论如下表,请参与他们的探究并完成所缺内容.
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞试液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量 稀盐酸 | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和的M溶液 | 出现白色沉淀 | 猜想成立 |
②乙、丙同学认为甲同学的实验方案不正确,其理由是碳酸钠溶液和氢氧化钙溶液也呈碱性.
| 物质 | CO2 | O2 | H2O | W |
| 反应前的质量(g) | 2 | 98 | 5 | 51 |
| 反应后的质量(g) | X | 2 | 59 | 5 |
| A. | 该反应是化合反应 | |
| B. | X的值是88 | |
| C. | W是一种由碳、氢、氧三种元素组成的化合物 | |
| D. | W是一种只由碳、氢两种元素组成的化合物 |
 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.