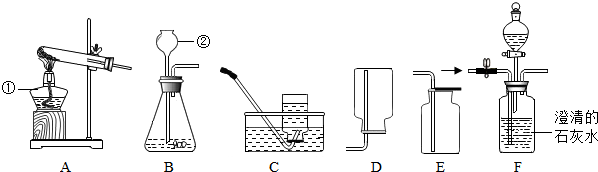
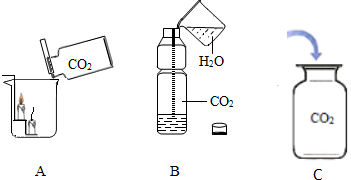
题目内容
11.已知某物质的化学式为RO3,其中R元素占40%,试确定R的名称和RO3的相对分子质量.分析 设R的相对原子质量是x,根据R元素的质量分数为40%可列出方程,解方程即可求解;由求得的R的相对原子质量和氧原子的相对原子质量是16,可求得RO3的相对分子质量.
解答 解:设R的相对原子质量是x,则
$\frac{x}{x+16×3}×100%$=40%
x=32
则R的名称为:硫;
RO3的相对分子质量为:32+16×3=80.
故填:硫;80.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
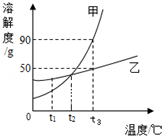 作图法是常用的数据处理方法,甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
作图法是常用的数据处理方法,甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题: