题目内容
8.粗盐中含有 MgCl2、CaCl2 等杂质,提纯粗盐的工艺流程如图,请回答问题.
(1)步骤①中发生的化学反应方程式是Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;
(2)步骤②加入过量的碳酸钠溶液的作用是除去CaCl2和过量的Ca(OH)2;
(3)操作 a 的名称是过滤;
( 4 ) 现 有 50g 质 量 分 数 为 10% 的 Na Cl 溶 液,如 若 将 上述溶液稀释为浓度 4% Na Cl 溶 液,需 要 水 的 质 量 是75g.
分析 氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;过滤能够把固体和液体分离;溶液稀释前后,溶质质量不变.
解答 解:(1)步骤①中氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,发生的化学反应方程式是:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓.
故填:Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓.
(2)步骤②加入过量的碳酸钠溶液的作用是除去CaCl2和过量的 Ca(OH)2.
故填:除去CaCl2和过量的 Ca(OH)2.
(3)操作a的名称是过滤,通过过滤把沉淀和液体分离.
故填:过滤.
(4)设需要水的质量为x,
根据题意有:50g×10%=(50g+x)×4%,
x=75g,
故填:75.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
18.下列关于碱的性质的叙述中错误的是( )
| A. | 向碱溶液中滴入紫色石蕊试液,石蕊试液变蓝 | |
| B. | 非金属氧化物都能跟碱反应生成盐和水 | |
| C. | 非金属氧化物都能跟碱反应生成盐和水,但不是中和反应 | |
| D. | 碱溶液可与某些盐发生反应 |
19.100克溶质质量分数为8%的食盐水,蒸发掉一定量的水后,溶质质量分数增大为16%,则蒸发掉水的质量为( )
| A. | 50克 | B. | 5克 | C. | 80克 | D. | 8克 |
16.我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等.小明灼烧棉 花、羊毛、涤纶三种纤维闻到如下表所示气味.则棉花、羊毛的编号分别为( )
| 纤维编号 | ① | ② | ③ |
| 灼烧时的气味 | 特殊气味 | 烧纸气味 | 烧焦羽毛气味 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②① |
3.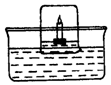 如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )
如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )
 如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )
如图,为得知空气中氧气的大致体积分数,用一只干冷的烧杯,沿水面罩住漂浮在水面燃烧的蜡烛.烧杯壁上很快出现小水珠,烧杯底变成黑色(即产生烟炱).不一会儿,蜡烛自动熄灭,杯内水位上升.待冷却后,发现上升部分水的体积约占烧杯容积的1/5,关于该实验的说法错误的是( )| A. | 现象的发生跟大气压强及气体的溶解性等有关 | |
| B. | 化学能转化为光能和热能,有熔化、液化等现象发生 | |
| C. | 实验说明,空气中氧气体积约占$\frac{1}{5}$ | |
| D. | 通过该实验还可证明蜡烛中肯定含有碳、氢、氧二种元素 |
17.Cu-Zn合金外观类似黄金.甲、乙、丙三位同学分别取Cu-Zn合金粉末与某稀硫酸反应,所得数据如表:
计算:
( 1 )金属混合物中锌的质量分数.
( 2 )该硫酸中溶质的质量分数.
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量(/g) | 10 | 10 | 20 |
| 取用稀硫酸的质量(/g) | 100 | 200 | 200 |
| 充分反应后过滤得到干燥固体的质量(/g) | 3.5 | 2 | 7 |
( 1 )金属混合物中锌的质量分数.
( 2 )该硫酸中溶质的质量分数.
18.化学变化的本质特征是( )
| A. | 有发光放热现象 | B. | 有颜色变化 | ||
| C. | 有新物质生成 | D. | 有气体或沉淀生成 |
 (1)有H、O、C、Na四种元素,请选用其中的一种或几种元素填写符合下列要求的化学式(各写一个):
(1)有H、O、C、Na四种元素,请选用其中的一种或几种元素填写符合下列要求的化学式(各写一个):