题目内容
9.将31克稀硫酸加入40克浓度为10%的氢氧化钠溶液中,求充分反应后所得溶液中溶质的质量分数.分析 根据溶质质量分数公式以及化学方程式进行计算,氢氧化钠能与硫酸反应生成硫酸钠和水,据此分析解答即可.
解答 解:所用氢氧化钠溶液中溶质的质量为40g×10%=4g;
设生成硫酸钠的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 142
4g x
$\frac{80}{142}$=$\frac{4g}{x}$
得:x=7.1g
反应后生成硫酸钠溶液的质量分数为:$\frac{7.1g}{31g+40g}$×100%=10%.
答:反应后生成硫酸钠溶液的质量分数为10%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
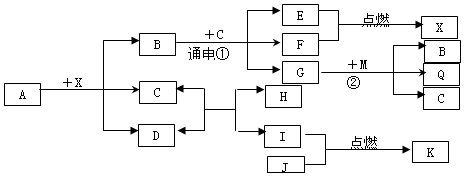
17.A、B、C、D是初中化学常见的物质,在一定条件下四种物质存在如下所示的转化关系A+B→C+D,则下列说法正确的是( )
| A. | 若A是金属,D是单质,B一定是酸 | |
| B. | 若A、C、D是化合物,B一定是化合物 | |
| C. | 若A、B、C分别是酸、碱、水,D一定是盐 | |
| D. | 若A、C都是金属,B是盐,A的活动性一定比C的活动性弱 |
4.如图为A、B、C为三种物质的溶解度曲线,下列说法正确的是( )
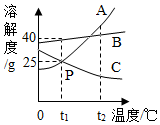

| A. | A和C的溶解度相等 | |
| B. | t2℃时,将A和C的混合溶液(两者均已达到饱和)降温至t1℃,析出晶体含有A和C | |
| C. | t2℃时,将A、B、C的饱和溶液分别降温至t1℃,所得溶液中溶质质量分数的大小关系是B>A>C | |
| D. | t1℃时,欲用A的饱和溶液配制10%的A溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器 |
14.下列说法错误的是( )
| A. | 在钢铁冶炼中,进行富氧鼓风可提高炉温,加速冶炼过程,提高钢铁的质量 | |
| B. | 氧气是化工生产和宇宙航行中的重要燃料 | |
| C. | 氮气在食品贮存时可用作保护气 | |
| D. | 稀有气体化学性质很不活泼,但也可以与某些物质发生化学反应 |
18.下列图象能正确反映对应变化关系的是( )
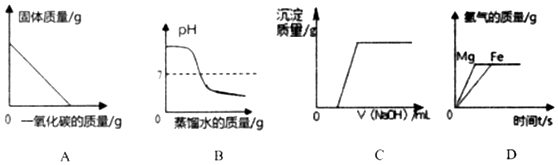

| A. | 实验室中用一氧化碳还原氧化铁 | |
| B. | 往氢氧化钙溶液中逐渐加入蒸馏水 | |
| C. | 向含有稀盐酸和氯化铜的混合溶液中滴加NaOH溶液 | |
| D. | 将等质量的镁粉和铁粉,分别放入两份溶质质量分数相同且足量的稀盐酸中 |
19.下列实验操作正确的是( )
| A. | 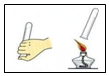 检验氢气的纯度 | B. |  用镊子取用碳酸钠粉末 | ||
| C. |  用活性炭净水时上端进水 | D. |  用广口瓶贮存少量氧气 |
 干电池在生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题:
干电池在生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题: