题目内容
9.写出下列反应的化学方程式,并在括号内注明基本反应类型:(1)过氧化氢溶液中加入硫酸铜2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑,(分解)反应;
(2)生石灰投入水中CaO+H2O═Ca(OH)2,(化合)反应;
(3)一氧化碳高温还原四氧化三铁Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)过氧化氢溶液中加入硫酸铜,硫酸铜作催化剂,反应的化学方程式为2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑;该反应符合“一变多”的特征,属于分解反应.
(2)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;该反应符合“多变一”的特征,属于化合反应.
(3)一氧化碳高温还原四氧化三铁生成铁和二氧化碳,反应的化学方程式为:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
故答案为:(1)2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑;分解;(2)CaO+H2O═Ca(OH)2;化合;(3)Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
相关题目
20.在学习化学过程中,我们会发现许多具有一定规律性的知识.下列叙述中,正确的是( )
| A. | 酸与金属反应一定生成氢气 | B. | 酸的组成中一定含有氧元素 | ||
| C. | 酸、碱、盐之间都能发生复分解反应 | D. | 置换反应不一定都要在溶液中进行 |
4.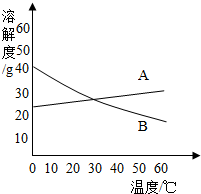 如图是A、B两种固体物质的溶解度曲线,下列叙述正确的是( )
如图是A、B两种固体物质的溶解度曲线,下列叙述正确的是( )
 如图是A、B两种固体物质的溶解度曲线,下列叙述正确的是( )
如图是A、B两种固体物质的溶解度曲线,下列叙述正确的是( )| A. | 10℃时,A的溶解度大于B的溶解度 | |
| B. | 20℃时,将20g B加入50g水中充分溶解,得溶液的质量为70g | |
| C. | 若使A物质从它的饱和溶液中大量析出,最适宜的方法是蒸发 | |
| D. | 50℃时,B物质饱和溶液中溶质的质量分数是20% |
14.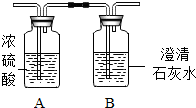 做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集气体样品并除去醋酸气体后,用如图实验装置进行探究.将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生.(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有二氧化碳和水蒸气;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测①二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②二氧化碳可能是由醋酸和碳酸氢钠反应生成的;
针对以上猜测,小明设计了以下实验:(请你填写如表)
Ⅲ、查阅资料:在百度网页中输入碳酸氢钠的化学性质,可以获知碳酸氢钠受热易分解,产物中有碳酸钠生成.再根据实验Ⅰ写出碳酸氢钠受热分解的化学方程式2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:取少量白色粉末,滴加稀盐酸,产生无色气体,并将气体通入澄清石灰水,石灰水变浑浊,则证明白色粉末为碳酸钠;
方法二:取少量白色粉末溶于水,加入适量氢氧化钙溶液,观察到溶液变浑浊,则证明白色粉末为碳酸钠.(其他合理答案均可).
 做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集气体样品并除去醋酸气体后,用如图实验装置进行探究.将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生.(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有二氧化碳和水蒸气;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测①二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②二氧化碳可能是由醋酸和碳酸氢钠反应生成的;
针对以上猜测,小明设计了以下实验:(请你填写如表)
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取碳酸氢钠样品少许加入试管中,加热到不产生气体为止,并把产生的气体通入澄清石灰水 | 试管口有小水滴产生 澄清石灰水变浑浊 | 猜想①正确 |
| 实验2 | 取碳酸氢钠样品少许加入试管中,滴入适量醋酸,并把产生的气体通入澄清石灰水 | 产生气泡,样品逐渐消失,澄清石灰水变浑浊 | 猜想②正确 |
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:取少量白色粉末,滴加稀盐酸,产生无色气体,并将气体通入澄清石灰水,石灰水变浑浊,则证明白色粉末为碳酸钠;
方法二:取少量白色粉末溶于水,加入适量氢氧化钙溶液,观察到溶液变浑浊,则证明白色粉末为碳酸钠.(其他合理答案均可).
1.维生素C是生命活动中不可缺少的营养物质,不同的饮料中维生素C的含量不同.下面是小明同学运用学到的实验方法测定橙汁、果味饮料中维生素C的含量.
【实验目的】测定不同饮料中维生素 C 的含量.
【实验原理】( l )维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色;
( 2 )淀粉遇到碘水变蓝色.
【实验试剂】碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水
【实验过程】步骤 1:在 4 支试管中分别盛有3.0mL的下列物质:①蒸馏水,②标准维生素 C 溶液,③橙汁,④果味饮料.分别向 4 支试管中滴加 2 滴淀粉溶液.
步骤 2:用 4 支相同的胶头滴管分别向 ①一 ④支试管中逐滴滴加碘水至刚好变色,并记录滴数.
【实验记录】
试回答下列问题:
( 1 )你认为小明测定的两种饮料中,③的维生素 C 的含敏较高;
( 2 )有的同学认为测定标准维生素 C 溶液是多余的,你认为呢?请说明理由不是多余的,因为测定标准维生素C溶液是确定维生素C含量的标准,以便估算出饮料中维生素C的浓度:( 3 )化学实验需要控制变量.下列ABD(填序号)情况会影响到测定结果.
A、每次实验所用饮料的颜色不同 B、量取的被测试物质的体积不同
C、试管的大小不同 D、没有用同一规格的胶头滴竹滴加碘水
【回顾与反思】实验中所用的淀粉溶液的作用是验证维生素C是否与碘水完全反应.
【实验目的】测定不同饮料中维生素 C 的含量.
【实验原理】( l )维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色;
( 2 )淀粉遇到碘水变蓝色.
【实验试剂】碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水
【实验过程】步骤 1:在 4 支试管中分别盛有3.0mL的下列物质:①蒸馏水,②标准维生素 C 溶液,③橙汁,④果味饮料.分别向 4 支试管中滴加 2 滴淀粉溶液.
步骤 2:用 4 支相同的胶头滴管分别向 ①一 ④支试管中逐滴滴加碘水至刚好变色,并记录滴数.
【实验记录】
| 测定物质 | ① | ② | ③ | ④ |
| 滴入碘水的数量(滴) | 1 | 8 | 15 | 5 |
( 1 )你认为小明测定的两种饮料中,③的维生素 C 的含敏较高;
( 2 )有的同学认为测定标准维生素 C 溶液是多余的,你认为呢?请说明理由不是多余的,因为测定标准维生素C溶液是确定维生素C含量的标准,以便估算出饮料中维生素C的浓度:( 3 )化学实验需要控制变量.下列ABD(填序号)情况会影响到测定结果.
A、每次实验所用饮料的颜色不同 B、量取的被测试物质的体积不同
C、试管的大小不同 D、没有用同一规格的胶头滴竹滴加碘水
【回顾与反思】实验中所用的淀粉溶液的作用是验证维生素C是否与碘水完全反应.
19. 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE(
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE( )膜,并采用新一代的氮化镓高亮度LED材料.下列说法正确的是( )
)膜,并采用新一代的氮化镓高亮度LED材料.下列说法正确的是( )
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE(
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE( )膜,并采用新一代的氮化镓高亮度LED材料.下列说法正确的是( )
)膜,并采用新一代的氮化镓高亮度LED材料.下列说法正确的是( )| A. | 钒氮合金高新钢属于纯净物 | |
| B. | 合金的熔点通常比主要成分金属高,硬度比成分金属小 | |
| C. | ETFE膜是一种易降解的有机高分子材料 | |
| D. | 已知镓(Ga)元素在化合物中显+3价,可推知氮化镓化学式为GaN |
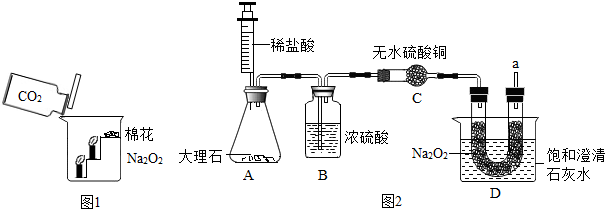
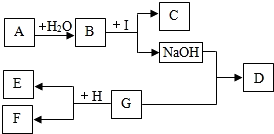 A-I为九年级化学所学的物质.已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,E、H为单质,F为浅绿色溶液,F、G、I均为只含有一种溶质的溶液.“→”表示物质间存在着相互转化的关系(部分生成物末标出),如图所示.请回答下列问题:
A-I为九年级化学所学的物质.已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,E、H为单质,F为浅绿色溶液,F、G、I均为只含有一种溶质的溶液.“→”表示物质间存在着相互转化的关系(部分生成物末标出),如图所示.请回答下列问题: