题目内容
10.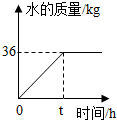 在工业上常用电石渣处理电电镀厂排出的酸性废水,已知电石渣的主要成分为氢氧化钙,若现有一堆含氢氧化钙80%的电石渣,恰好处理了含有73kg的HCl的废水(假设电石渣中的杂质,废水中其他成分均不参加反应),生成水的质量与时间的关系如图所示,求:
在工业上常用电石渣处理电电镀厂排出的酸性废水,已知电石渣的主要成分为氢氧化钙,若现有一堆含氢氧化钙80%的电石渣,恰好处理了含有73kg的HCl的废水(假设电石渣中的杂质,废水中其他成分均不参加反应),生成水的质量与时间的关系如图所示,求:(1)反应结束后,生产水的总质量为36kg;
(2)电石渣的质量.
分析 (1)根据图示可知反应结束后,生产水的总质量为36Kg进行分析解答.
(2)由水的质量,根据反应的化学方程式计算出需要电石渣的质量即可.
解答 解:(1)根据图示可知反应结束后,生产水的总质量为36Kg;
(2)设电石渣中氢氧化钙的质量为x
Ca(OH)2+H2SO4═CaSO4+2H2O
74 36
x 36Kg
$\frac{74}{x}=\frac{36}{36Kg}$
x=74Kg
电石渣的质量=$\frac{74Kg}{80%}$=92.5Kg
答案:
(1)36;
(2)电石渣的质量为92.5Kg
点评 本题难度不大,掌握根据化学方程式的计算、化学式的有关计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
20.下列有关实验现象的描述,正确的是( )
| A. | 白磷在空气中燃烧产生大量白雾 | |
| B. | 硫在氧气中燃烧,产生蓝紫色火焰 | |
| C. | 细铁丝在氧气中燃烧,火星四射,生成红棕固体 | |
| D. | 铁与稀硫酸反应有气泡产生,溶液由无色变成黄色 |
5.分析推理是一种重要的学习方法,善于运用分析推理可以使我们更快的理解所学的知识,提高我们的学习效率,下列关于一些知识的分析推理中,正确的是( )
| A. | 组成石墨和金刚石的原子相同,而金刚石硬度很大,所以石墨的硬度也很大 | |
| B. | 力的作用是相互的,所以晓铭推墙的力的大小一定等于他所受的重力 | |
| C. | 碱溶液中含有氢元素,所以含有氢元素的就是碱 | |
| D. | 水和冰的化学式相同,所以组成水和冰的分子是同一种分子 |
5.天然气中含有H2S等有毒气体,如图为天然气合成氨的工艺流程.下列说法正确的是(提示:2H2S+3O2 $\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O)( )
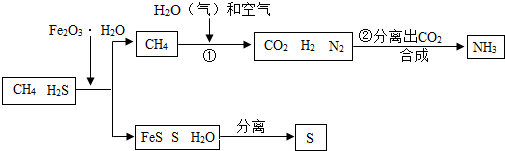

| A. | 该工艺中除去了H2S,有控制酸雨的意义 | |
| B. | 合成氨反应中的N2与 H2的质量比是1?3 | |
| C. | 使用Fe2O3•H2O除去H2S反应中只有一种元素的化合价发生了变化 | |
| D. | ①中的反应可表示为:CH4+2H2O $\frac{\underline{\;高温\;}}{\;}$CO2+4H2 |
9.下列关于纸张的性质,属于其化学性质的是( )
| A. | 可燃 | B. | 白色 | C. | 易撕碎 | D. | 不溶于水 |
10.在常温下,测得相同溶质质量分数的下列四种溶液 PH 的大小情况为:HCl<H2SO4<H2S<H2CO3.通过复分解反应,用较强酸可制得某些较弱酸,下列四个反应中不符合该规律的是( )
| A. | HCl+NaHCO3═NaCl+CO2↑+H2O | B. | 2HCl+CaS═CaCl2+H2S↑ | ||
| C. | H2S+CuSO4═H2SO4+CuS↓ | D. | 2HCl+CaCO3═CaCl2+CO2↑+H2O |
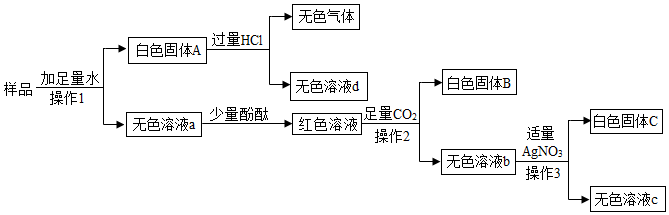
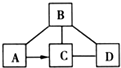 已知A-D是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐.它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)
已知A-D是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐.它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)