题目内容
2.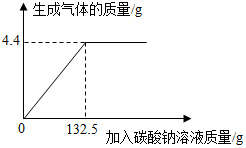 向一定质量、一定溶质质量分数和稀盐酸中逐滴加入某碳酸钠溶液,实验过程中,产生气体质量与加入碳酸钠溶液的质量关系如图所示,试计算:
向一定质量、一定溶质质量分数和稀盐酸中逐滴加入某碳酸钠溶液,实验过程中,产生气体质量与加入碳酸钠溶液的质量关系如图所示,试计算:(1)恰好完全反应时,生成气体的质量为4.4g
(2)所加碳酸钠溶液的溶质质量分数是多少?
分析 由图可以看出恰好反应时生成的气体的质量,根据二氧化碳的质量和碳酸钠与盐酸反应生成氯化钠、水和二氧化碳的化学方程式求算出碳酸钠的质量,进而求算溶液中碳酸钠的质量分数.
解答 解:根据题目给出的图很直观可以得出生成的二氧化碳的质量为4.4g.
设反应的碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{44}$=$\frac{x}{4.4g}$
x=10.6g
则所加碳酸钠溶液中碳酸钠的质量分数为$\frac{10.6g}{132.5g}$×100%=8%
答:(1)恰好完全反应时,生成气体的质量为4.4g
(2)所加碳酸钠溶液的溶质质量分数是8%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
10.下列实验操作正确的是( )
| A. |  测溶液pH | B. |  闻气体气味 | C. | 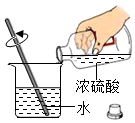 稀释浓硫酸 | D. |  点燃酒精灯 |
7.下列有关化学观念的叙述错误的是( )
| A. | 爱因斯坦体内的某个原子现在可能在你的身体里 | |
| B. | 通过化学变化,人们改造物质世界并实现物质与能量的相互转化 | |
| C. | 用刀切苹果的过程中,个别原子被分成了更小的微粒 | |
| D. | 运用分类的方法,可根据物质所属的类别预测物质的性质 |
14.下列物质属于纯净物的是( )
| A. | 干冰 | B. | 矿泉水 | C. | 清新空气 | D. | 大理石 |
12.下列事实描述中,属于物质化学性质的是( )
| A. | 干冰易升华 | B. | 氮气难溶于水 | ||
| C. | 金刚石是最硬的物质之一 | D. | 粮食能够酿酒 |
