题目内容
11.向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉,充分反应后过滤得到溶液A和固体B,滤液A中所含的溶质不可能的情况是( )| A. | Zn(NO3)2、Cu(NO3)2 | B. | Zn(NO3)2、Cu(NO3)2、AgNO3 | ||
| C. | Zn(NO3)2、AgNO3 | D. | Zn(NO3)2 |
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此进行分析判断.
解答 解:由于金属的活动性是锌>铜>银、向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉,锌先与硝酸银溶液反应生成硝酸锌溶液和银,当银离子被全部置换出来,若有锌剩余,才能继续与硝酸铜溶液发生置换反应,生成硝酸锌溶液和铜.
A、若溶液中的硝酸银前后被完全置换,则此时溶液中的溶质是Zn(NO3)2、Cu(NO3)2,此种情况可能存在,故选项不符合题意;
B、溶液中含有硝酸银,则银离子还没有被全部置换出来,硝酸铜还没参加反应,则此时溶液中的溶质是Zn(NO3)2、Cu(NO3)2、AgNO3,此种情况可能存在,故选项不符合题意.
C、溶液中含有硝酸银,则银离子还没有被全部置换出来,硝酸铜还没参加反应,则此时溶液中的溶质是Zn(NO3)2、Cu(NO3)2、AgNO3,滤液A中所含的溶质不可能为Zn(NO3)2、AgNO3,故选项符合题意.
D、若锌是足量的,能与硝酸银、硝酸铜溶液完全反应,则此时溶液中的溶质是Zn(NO3)2,此种情况可能存在,故选项不符合题意.
故选:C.
点评 本题难度不大,掌握金属的化学性质(尤其是当同一种金属同时能置换两种活动性较弱的金属时,首先被置换出来的是金属活动性最弱的金属)是正确解答本题 的关键.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
5.下列关于空气各成分的说法中,错误的是( )
| A. | 空气中氧气的体积分数约为21% | |
| B. | 氦气化学性质不活泼,可用于食品防腐 | |
| C. | 二氧化碳在空气中的含量增多会对空气造成污染 | |
| D. | 空气中的稀有气体一般不跟其他物质反应,又被称为“惰性气体” |
2.下列说法中正确的是( )
| A. | 在常温下所有的金属都是固体 | |
| B. | 物质的性质是决定物质用途的唯一因素 | |
| C. | 合金中不一定含有金属 | |
| D. | 一般来说,合金比组成它的纯金属硬度大,强度高,熔点低 |
6.逻辑推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 溶液一定是均一稳定的,但均一稳定的物质不一定是溶液 | |
| B. | 有机物都含有碳元素,所以含有碳元素的化合物一定都是有机物 | |
| C. | 铝比铁活泼,所以铝的抗腐蚀性能一定比铁差 | |
| D. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
16.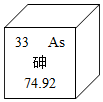 据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )
据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )
 据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )
据新华网报道,英国某研究机构指出大米含致癌物质砷,专家建议4岁半以下儿童不应以米浆取代奶粉或人奶,以免摄取过量的砷.砷的部分信息如图,则说法正确的是( )| A. | 砷属于金属元素 | B. | 砷原子的最外层电子数是33 | ||
| C. | 砷原子的质子数是33 | D. | 砷的相对原子质量是74.92 |
20.下列物质鉴别方法,错误的是( )
| A. | 用澄清石灰水鉴别CO和CO2 | B. | 用MnO2鉴别蒸馏水和过氧化氢溶液 | ||
| C. | 用紫色石蕊纸花鉴别水和碳酸饮料 | D. | 用燃着的木条鉴别H2和CH4 |