题目内容
11.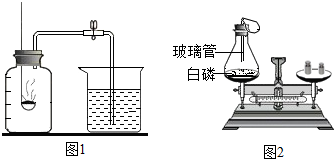 上册化学教材已经两次运用了红磷的燃烧进行实验探究,其所用装置如图所示,请按要求回答下列问题:
上册化学教材已经两次运用了红磷的燃烧进行实验探究,其所用装置如图所示,请按要求回答下列问题:(1)写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
(2)图1和图2实验探究的目的分别是什么?图1实验探究的目的是测定空气中氧气的含量;图2实验探究的目的是验证质量守恒定律
(3)对两个实验装置的共同要求是什么?装置气密性要好(一点即可)
(4)图1实验时,测定结果偏小,其可能原因是什么?装置漏气(一点即可)
分析 (1)根据红磷燃烧生成五氧化二磷解答;
(2)根据题中信息及图示分析解答;
(3)根据实验特点分析解答;
(4)利用红磷燃烧测定空气中氧气的含量时,如果操作不当,会导致测定的结果不准确.
解答 解:(1)红磷燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 ;
(2)图1实验探究的目的是测定空气中氧气的含量;图2实验探究的目的是验证质量守恒定律;
(3)为保证实验结果的准确性,对两个实验装置的共同要求是装置气密性要好;
(4)如果装置漏气,红磷不足,没有冷却到室温就打开止水夹,都能够导致进入集气瓶中水的体积不到总容积的五分之一.
答案:
(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 ;
(2)图1实验探究的目的是测定空气中氧气的含量;图2实验探究的目的是验证质量守恒定律;
(3)装置气密性要好;
(4)装置漏气.
点评 本题考查了测定空气中氧气的体积分数的有关问题,知识面较广,关键是了解用红磷测定氧气在空气中含量的实验的注意事项、了解实验数据的处理或者误差分析的方法及技巧及常见气体的制取装置、收集方法等的选择等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.如图是X、Y、Z、W四种溶液的近似pH.下列判断不正确的是( )
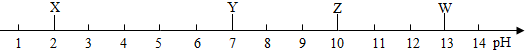
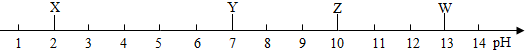
| A. | X一定能使石蕊溶液变红 | B. | Y一定是水 | ||
| C. | Z一定能使酚酞溶液变红 | D. | W的碱性一定比Z强 |
6.下列各组物质的区分方法中,不可行的是( )
| A. | 硬水、软水--加肥皂水,搅拌观察泡沫的多少 | |
| B. | 羊毛纤维、涤纶--灼烧,闻气味 | |
| C. | 氢氧化钠、氢氧化镁--加水观察 | |
| D. | 氯化钠、氢氧化钠--加稀盐酸区分 |
3.对比分析是化学研究和学习基本方法.甲、乙、丙三位同学利用图中的装置,围绕“用称量的方法验证化学反应是否遵守质量守恒定律并分析实验条件”这一探究目的开展活动.
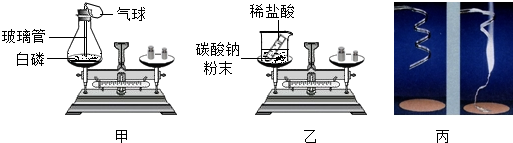
【实验步骤】
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在两个托盘天平上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别利用装置进行化学反应.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
(2)比较甲、丙同学的实验有许多相似之处,如生成物都属于下列选项中的B.
A、酸 B、氧化物 C、碱 D、盐
(3)通过对上述实验的对比分析,甲乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有反应前未称量参加反应的氧气的质量,反应后生成的氧化镁部分外溢,无法称量.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】(4)请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类、数目、质量都没有发生改变.

【实验步骤】
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放在两个托盘天平上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别利用装置进行化学反应.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘天平上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | |||
| 甲同学 | ①白磷燃烧,产生浓浓的白烟,放出热量,气球先变大后又变小,天平平衡 | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | 该反应遵守质量守恒定律 |
| 乙同学 | ②烧杯内产生大量气泡,天平不平衡 | ③Na2CO3+2HCl=2NaCl+H2O+CO2↑ | 该反应遵守质量守恒定律 |
| 丙同学 | 镁条剧烈燃烧,发出耀眼白光,放热,生成 白色固体.反应前后称量质量不相等. | ④2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 该反应不遵守质量守恒定律 |
A、酸 B、氧化物 C、碱 D、盐
(3)通过对上述实验的对比分析,甲乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有反应前未称量参加反应的氧气的质量,反应后生成的氧化镁部分外溢,无法称量.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】(4)请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类、数目、质量都没有发生改变.
1.与氢氧根具有相同质子数和电子数的微粒是( )
| A. | F- | B. | Cl- | C. | NH4+ | D. | NH3 |