题目内容
14.人体摄入锌不足会引起多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌口服液来补锌.已知葡萄糖酸锌的化学式为C12H22O14Zn.(1)葡萄糖酸锌中碳、氢两种元素的质量比为72:11.
(2)葡萄糖酸锌中锌元素的质量分数为14.3%(计算结果精确到0.1%).
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:(1)葡萄糖酸锌中碳、氢元素的质量比为(12×12):(1×22)=72:11.
(2)葡萄糖酸锌中锌元素的质量分数为$\frac{65}{12×12+1×22+16×14+65}×$100%≈14.3%.
故答案为:(1)72:11;(2)14.3%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2.下列物质之间不能发生化学反应的是( )
| A. | 石灰水与稀盐酸 | B. | 铜与硝酸银溶液 | C. | 银与稀硫酸 | D. | 二氧化碳与水 |
9.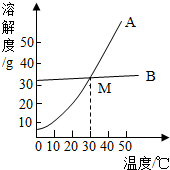 已知氯化钠、碳酸钠在不同温度时的溶解度如下:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:
(1)依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如图,图中能表示碳酸钠溶解度曲线的是A(填“A”或“B”).
(2)图中两溶解度曲线相交于M点,此点表示的意义是在30℃时氯化钠和碳酸钠的溶解度相等.
(3)40℃时,把50gA物质放入100g水中,充分搅拌,所得溶液是饱和溶液(填“饱和”或“不饱和”).
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理碳酸钠的溶解度随温度的降低减小明显.
 已知氯化钠、碳酸钠在不同温度时的溶解度如下:
已知氯化钠、碳酸钠在不同温度时的溶解度如下:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 10 | 18 | 36.5 | 50 | |
(2)图中两溶解度曲线相交于M点,此点表示的意义是在30℃时氯化钠和碳酸钠的溶解度相等.
(3)40℃时,把50gA物质放入100g水中,充分搅拌,所得溶液是饱和溶液(填“饱和”或“不饱和”).
(4)生活在盐湖(主要成分是NaCl和Na2CO3)附近的人们习惯“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”.请你答出“冬天捞碱”的道理碳酸钠的溶解度随温度的降低减小明显.
19.下列说法错误的是( )
| A. | 在钢铁表面涂油漆可以防止铁生锈 | |
| B. | 10mL酒精和10mL水混合后体积小于20mL,是因为分子变小了 | |
| C. | 扑灭森林火灾时,可开挖防火隔离带,其目的是隔绝可燃物 | |
| D. | 用铅锑合金制作保险丝,是因为熔点低 |
6.下列生活用品中,所使用的主要材料属于有机合成材料的是( )
| A. | 塑料脸盆 | B. | 纯棉毛巾 | C. | 玻璃茶杯 |
11.实验室有不纯的氯酸钾样品12.5g,把该样品与少量二氧化锰混合加热制取氧气(杂质不参加反应),充分反应后,$\underset{固}{•}\underset{体}{•}\underset{混}{•}\underset{合}{•}\underset{物}{•}\underset{质}{•}\underset{量}{•}$变化如下所示:
(1)生成氧气的质量为4.8g;
(2)氯酸钾在样品中的质量分数是多少?
| 反应前固体总质量 | 反应后固体总质量 |
| 13.5g | 8.7g |
(2)氯酸钾在样品中的质量分数是多少?
12.下列实验方案能够达到相应实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH4中是否含有H2 | 将气体点燃 |
| B | 鉴别NaOH溶液和Ca(OH)2溶液 | 分别向溶液中通入CO2 |
| C | 除去NaCl中的Na2CO3 | 向其中加入足量稀盐酸 |
| D | 比较铁和铜的活动顺序 | 将其分别加入ZnSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |