题目内容
如图是某种钙片的商品标签.江涛同学想知道碳酸钙含量标注是否属实,他取4 片钙片研碎放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共用盐酸40g;最后,烧杯中剩余物的质量为47.8g(假定钙片中的其它成分不与稀盐酸反应也不溶于水).请计算:
(1)通过计算判断钙片中的碳酸钙含量标注是否属实?
(2)他反应所用盐酸的溶质质量分数是多少?

【答案】分析:(1)测定过程中放出气体CO2使反应后剩余物质质量小于反应前各物质质量的总和,运用质量守恒定律计算出气体的质量;根据二氧化碳的质量求出碳酸钙的质量,标签标明每片含碳酸钙≥1.24g,根据测定数据计算出每片含碳酸钙的质量与标签对比,判断标注是否属实.
(2)根据二氧化碳的质量求出氯化氢质量,利用溶质质量分数的计算公式求出盐酸的溶质质量分数.
解答:解:根据质量守恒定律可知,生成C02的质量为:40g+4×2.5g-47.8g=2.2g.
(1)设参加反应的CaCO3的质量为x、
CaCO3+2HCl═CaCl2+H2O+C02↑
100 73 44
x y 2.2g
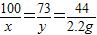
解得:x=5g y=3.65g
每片钙片中含碳酸钙的质量为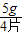 =1.25g/片>1.24g/片,故标注属实
=1.25g/片>1.24g/片,故标注属实
(2)所用盐酸的溶质质量分数=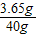 ×100%=9.125%
×100%=9.125%
答:(1)标注属实(2)所用盐酸的溶质质量分数为9.125%
故答案为:(1)标注属实(2)9.125%
点评:根据质量守恒定律计算出放出气体二氧化碳的质量是解决本题的关键.
(2)根据二氧化碳的质量求出氯化氢质量,利用溶质质量分数的计算公式求出盐酸的溶质质量分数.
解答:解:根据质量守恒定律可知,生成C02的质量为:40g+4×2.5g-47.8g=2.2g.
(1)设参加反应的CaCO3的质量为x、
CaCO3+2HCl═CaCl2+H2O+C02↑
100 73 44
x y 2.2g
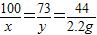
解得:x=5g y=3.65g
每片钙片中含碳酸钙的质量为
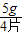 =1.25g/片>1.24g/片,故标注属实
=1.25g/片>1.24g/片,故标注属实(2)所用盐酸的溶质质量分数=
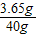 ×100%=9.125%
×100%=9.125%答:(1)标注属实(2)所用盐酸的溶质质量分数为9.125%
故答案为:(1)标注属实(2)9.125%
点评:根据质量守恒定律计算出放出气体二氧化碳的质量是解决本题的关键.

练习册系列答案
相关题目
 如图是某种钙片的商品标签.江涛同学想知道碳酸钙含量标注是否属实,他取4 片钙片研碎放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共用盐酸40g;最后,烧杯中剩余物的质量为47.8g(假定钙片中的其它成分不与稀盐酸反应也不溶于水).
如图是某种钙片的商品标签.江涛同学想知道碳酸钙含量标注是否属实,他取4 片钙片研碎放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共用盐酸40g;最后,烧杯中剩余物的质量为47.8g(假定钙片中的其它成分不与稀盐酸反应也不溶于水).