题目内容
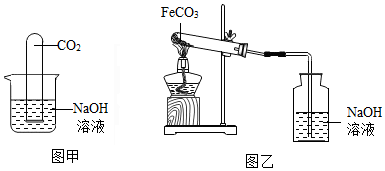
9.“锡纸”和“铝箔”都曾用于烧烤食品.这两种物质的性质如何呢?小安进行如下实验:如图,在天平左右两个托盘上各放一个大小相同的烧杯,在烧杯中分别盛有相同质量且溶质质量分数为19.6%的稀硫酸各200克,调节天平至平衡.然后,向左、右两只烧杯中分别同时加入相同质量的“铝箔”和“锡纸”.天平的指针偏向(√表示指针偏转方向)如表所示:
| 时间 | 铝箔(左) | 中间 | 锡纸(右) |
| 反应开始前 | √ | ||
| 1分钟后 | √ | ||
| 2分钟后 | √ | ||
| 反应结束后 | √ |
【查阅资料】锡的化学性质很稳定,在常温下不易与氧气反应,能与硫酸反应,化学方程式为:Sn+H2SO4═SnSO4+H2↑;铝在空气中表面会形成致密的氧化膜.
(1)本实验中右边锡纸与稀硫酸反应共产生了0.8克的氢气.
(2)根据反应的整个过程,请在坐标图2上画出铝和稀硫酸反应产生氢气的质量随时间变化的大致曲线.
分析 (1)根据实验结束后,两烧杯中都有大量的金属剩余,说明稀硫酸完全反应进行分析;
(2)根据表中天平的指针偏向的方向进行分析.
解答 解:(1)实验结束后,两烧杯中都有大量的金属剩余,说明稀硫酸完全反应,依据质量守恒定律可知,本实验中右边锡纸与稀硫酸反应共产生的氢气质量为:$\frac{2}{98}$×19.6%×200g=0.8g;
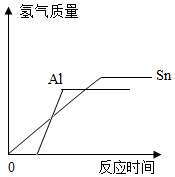
(2)依据表中天平的指针偏向的方向可知,铝和稀硫酸反应产生氢气的质量随时间变化的大致曲线,如图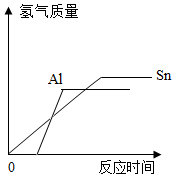
故答案为:(1)0.8g;
(2)
点评 本题主要考查了金属的化学性质,难度不大,需要在平时的学习中加强训练即可完成.

练习册系列答案
相关题目
12.下列做法与对应的化学方程式均正确的是( )
| A. | 用稀盐酸除去铁制品表面的铁锈:FeO+2HCl=FeCl2+H2O | |
| B. | 用硫酸洗去试管壁上附着的铜:Cu+H2SO4=CuSO4+H2↑ | |
| C. | 铝溶于稀硫酸:4Al+6H2SO4=2Al(SO4)3+6H2↑ | |
| D. | 在实验室制取CO2:CaCO3+2HCl=CaCl2+H2O+CO2↑ |
17.工业上用天然气和水蒸气在高温条件下发生反应得到CO和H2,该反应的化学方程式为CH4+H2O=CO+3H2,得到的CO 和H2的混合气被称为合成气,合成气在工业上可用于合成一系列化工原料和新型燃料,还可用于冶炼某些金属.某化学兴趣小组的同学在实验室模拟了合成气的制备,并设计实验验证合成气的还原性.用合成气还原足量氧化铜,实验装置如图1所示:

【设计买验步骤】
①连接好装置并检查气密性. ②装入药品,分别称量装置D、E的质量.
③连接好装置,通入合成气一段时间. ④缓缓通入合成气,加热装置C,使其充分反应.
⑤停止加热,继续通入合成气至恢复到室温.⑥再次分别称量装置D、E的质量.
【完善实验设计】
经过讨论同学们认为,装置E后还应添加一个酒精灯,并在实验步骤②(填实验步骤
的序号)中点燃(点燃前应对气体验纯).
【进行实验】该小组的同学按上述步骤进行实验,并记录了实验现象和数据:
①装置C中出现红色物质.
②称量数据如表所示.
【现象分析和数据处理】
①甲同学根据装置C中的现象,认为是合成气中的CO和H2还原了CuO.
②乙同学通过对上表数据的分析,推测除了CO和H2以外,制得的合成气中可能还有未反应的CH4,且CH4也还原了CuO.试通过计算说明他的推测依据.
③丙同学提出,实验步骤⑤中通入的气体会带走装置E中的部分水蒸气,使实验产生误差.你认为该误差对乙同学的推测结果是否有影响?否
因为带走水蒸气会使测得的CO2质量偏低,而实际测得的生成物中碳、氢元素的质量比已经大于2:1,所以对推测结果无影响 (选填“是”或“否”,并说明理由).
【拓展探究】该小组同学对于CH4是否真的能够还原氧化铜提出了质疑并进行探究.
查阅资料:甲烷具有还原性,可以还原氧化铜,生成CO2和H2O;
白色的无水硫酸铜遇水会变成蓝色.
实验设计:该小组同学拟用纯净的甲烷气体和如图2装置进行实验.
①图2装置F中盛放的试剂名称是澄清石灰水.
②图2装置的正确连接顺序是HGFI(填字母,且每套装置限用一次).
实验反思:除了可能是CH4也还原了CuO外,出现上表数据关系还可能是因为因为根据测得数据计算,生成物中碳、氧元素的质量比值2:1,所以可能是合成气中参与反应的CO与H2的分子个数比大于1:3(或H2未完全参加反应、生成的水未被完全吸收等)
不用填(写出一个原因,并说明理由).

【设计买验步骤】
①连接好装置并检查气密性. ②装入药品,分别称量装置D、E的质量.
③连接好装置,通入合成气一段时间. ④缓缓通入合成气,加热装置C,使其充分反应.
⑤停止加热,继续通入合成气至恢复到室温.⑥再次分别称量装置D、E的质量.
【完善实验设计】
经过讨论同学们认为,装置E后还应添加一个酒精灯,并在实验步骤②(填实验步骤
的序号)中点燃(点燃前应对气体验纯).
【进行实验】该小组的同学按上述步骤进行实验,并记录了实验现象和数据:
| 装置D的质量 | 装置E的质量 | |
| 反应前 | 292.4g | 198.2g |
| 反应后 | 296.0g | 201.5g |
②称量数据如表所示.
【现象分析和数据处理】
①甲同学根据装置C中的现象,认为是合成气中的CO和H2还原了CuO.
②乙同学通过对上表数据的分析,推测除了CO和H2以外,制得的合成气中可能还有未反应的CH4,且CH4也还原了CuO.试通过计算说明他的推测依据.
③丙同学提出,实验步骤⑤中通入的气体会带走装置E中的部分水蒸气,使实验产生误差.你认为该误差对乙同学的推测结果是否有影响?否
因为带走水蒸气会使测得的CO2质量偏低,而实际测得的生成物中碳、氢元素的质量比已经大于2:1,所以对推测结果无影响 (选填“是”或“否”,并说明理由).
【拓展探究】该小组同学对于CH4是否真的能够还原氧化铜提出了质疑并进行探究.
查阅资料:甲烷具有还原性,可以还原氧化铜,生成CO2和H2O;
白色的无水硫酸铜遇水会变成蓝色.
实验设计:该小组同学拟用纯净的甲烷气体和如图2装置进行实验.
①图2装置F中盛放的试剂名称是澄清石灰水.
②图2装置的正确连接顺序是HGFI(填字母,且每套装置限用一次).
实验反思:除了可能是CH4也还原了CuO外,出现上表数据关系还可能是因为因为根据测得数据计算,生成物中碳、氧元素的质量比值2:1,所以可能是合成气中参与反应的CO与H2的分子个数比大于1:3(或H2未完全参加反应、生成的水未被完全吸收等)
不用填(写出一个原因,并说明理由).
1. 在表A、B、C三组选项中,有一组物质能够实现如图所示的转化,请回答下列问题.
在表A、B、C三组选项中,有一组物质能够实现如图所示的转化,请回答下列问题.
(1)选项中符合转化关系的是A(填序号“A”“B”或“C”).
(2)写出甲物质在生产或生活中的一种用途制取烧碱.
(3)由甲生成丙的反应现象是产生白色沉淀.
 在表A、B、C三组选项中,有一组物质能够实现如图所示的转化,请回答下列问题.
在表A、B、C三组选项中,有一组物质能够实现如图所示的转化,请回答下列问题. | 选项 | 甲 | 乙 | 丙 |
| A | Na2CO3 | CO2 | CaCO3 |
| B | NaOH | NaCl | NaNO3 |
| C | CuO | CuSO4 | Cu(OH)2 |
(2)写出甲物质在生产或生活中的一种用途制取烧碱.
(3)由甲生成丙的反应现象是产生白色沉淀.
16.下列化学方程式符合题目且书写正确的是( )
| A. | 不能用铁器盛放农药波尔多液的:2Fe+CuSO4═Fe(SO4)3+3Cu | |
| B. | 证明铜的活性比银强.Cu+2AgCl═CuCl2+2Ag | |
| C. | 用氢氧化钠溶液吸收有毒气体2NaOH+SO2═Na2SO4+H2O | |
| D. | 甲烷完全燃烧的方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |

 为测定空气里氧气的含量,甲、乙两个同学用如图所示的装置分别进行了实验探究.
为测定空气里氧气的含量,甲、乙两个同学用如图所示的装置分别进行了实验探究.