题目内容
请用所学化学知识解释下列原理.
(1)用过氧化氢制氧气,常加入少量的二氧化锰,是因为二氧化锰对该反应具有 作用.
(2)熄灭蜡烛,用嘴吹灭,其灭火的原理是什么?
(3)用化学方程式表示铜的活动性比银强的实验原理 .
(4)蜂窝煤在家用煤炉中充分燃烧时不仅看到煤块红热,还能看到上层有蓝色火焰.用化学方程式表示其中所发生的化学反应.
(1)用过氧化氢制氧气,常加入少量的二氧化锰,是因为二氧化锰对该反应具有
(2)熄灭蜡烛,用嘴吹灭,其灭火的原理是什么?
(3)用化学方程式表示铜的活动性比银强的实验原理
(4)蜂窝煤在家用煤炉中充分燃烧时不仅看到煤块红热,还能看到上层有蓝色火焰.用化学方程式表示其中所发生的化学反应.
考点:催化剂的特点与催化作用,一氧化碳的化学性质,金属的化学性质,书写化学方程式、文字表达式、电离方程式,灭火的原理和方法
专题:空气与水,金属与金属材料
分析:(1)从过氧化氢溶液在二氧化锰催化作用下生成水和氧气,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率去分析解答;
(2)从熄灭蜡烛,用嘴吹灭,降低了蜡烛的温度,降到蜡烛的着火点以后,蜡烛熄灭去分析解答;
(3)从要证明铜的活动性比银强,可以把铜丝放到硝酸银溶液中去.铜和硝酸银反应生成硝酸铜和银去分析解答;
(4)从蜂窝煤在家用煤炉中燃烧时.煤的主要成分碳和空气中的氧气在点燃的条件下反应生成二氧化碳;二氧化碳和碳在高温下反应生成一氧化碳,一氧化碳和氧气反应生成二氧化碳并发出蓝色火焰去分析解答;
(2)从熄灭蜡烛,用嘴吹灭,降低了蜡烛的温度,降到蜡烛的着火点以后,蜡烛熄灭去分析解答;
(3)从要证明铜的活动性比银强,可以把铜丝放到硝酸银溶液中去.铜和硝酸银反应生成硝酸铜和银去分析解答;
(4)从蜂窝煤在家用煤炉中燃烧时.煤的主要成分碳和空气中的氧气在点燃的条件下反应生成二氧化碳;二氧化碳和碳在高温下反应生成一氧化碳,一氧化碳和氧气反应生成二氧化碳并发出蓝色火焰去分析解答;
解答:解:(1)过氧化氢溶液在二氧化锰催化作用下生成水和氧气,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率,故二氧化锰是催化剂,所起的作用是催化作用;故答案为:催化;
(2)熄灭蜡烛,用嘴吹灭,降低了蜡烛的温度,降到蜡烛的着火点以后,蜡烛熄灭;故答案为:降温达到蜡烛的着火点以下;
(3)要证明铜的活动性比银强,可以把铜丝放到硝酸银溶液中去.铜和硝酸银反应生成硝酸铜和银,其化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag;故答案为:Cu+2AgNO3═Cu(NO3)2+2Ag;
(4)蜂窝煤在家用煤炉中燃烧时.煤的主要成分碳和空气中的氧气在点燃的条件下反应生成二氧化碳,其化学方程式为:C+O2
CO2;二氧化碳和碳在高温下反应生成一氧化碳,其化学方程式为:C+CO2
2CO;一氧化碳和氧气反应生成二氧化碳并发出蓝色火焰,其反应的化学方程式为:2CO+O2
2CO2;
故答案为:C+O2
CO2 C+CO2
2CO 2CO+O2
2CO2;
(2)熄灭蜡烛,用嘴吹灭,降低了蜡烛的温度,降到蜡烛的着火点以后,蜡烛熄灭;故答案为:降温达到蜡烛的着火点以下;
(3)要证明铜的活动性比银强,可以把铜丝放到硝酸银溶液中去.铜和硝酸银反应生成硝酸铜和银,其化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag;故答案为:Cu+2AgNO3═Cu(NO3)2+2Ag;
(4)蜂窝煤在家用煤炉中燃烧时.煤的主要成分碳和空气中的氧气在点燃的条件下反应生成二氧化碳,其化学方程式为:C+O2
| ||
| ||
| ||
故答案为:C+O2
| ||
| ||
| ||
点评:催化剂的定义可这样记忆:“一变二不变”指:一变指:改变其他物质的化学反应速率;二不变指:催化剂的质量和化学性质不变.

练习册系列答案
相关题目
下列生产过程主要发生物理变化的是( )
A、 沼气生产 |
B、 石油分馏 |
C、 转炉炼钢 |
D、 高炉炼铁 |
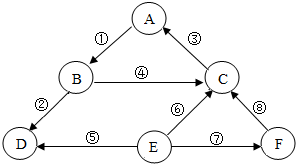 A~F是初中化学常见的6种物质,它们在一定条件下的转化关系如图所示(部分反应物或生成物已略去).已知A由一种元素组成,B、C由两种元素组成,D、E、F由三种元素组成.A、B、C、D、E、F均含有氧元素.E的水溶液呈碱性,①⑧表示8个不同的化学反应.
A~F是初中化学常见的6种物质,它们在一定条件下的转化关系如图所示(部分反应物或生成物已略去).已知A由一种元素组成,B、C由两种元素组成,D、E、F由三种元素组成.A、B、C、D、E、F均含有氧元素.E的水溶液呈碱性,①⑧表示8个不同的化学反应.