题目内容
3.下列不会加剧酸雨、臭氧层空洞、温室效应等环境问题的是( )| A. | 超音速飞机尾气排放 | B. | 使用太阳能沐浴器 | ||
| C. | 使用煤做燃料 | D. | 使用氟利昂做冰箱制冷剂 |
分析 根据造成酸雨(二氧化硫、氮氧化物的排放,以及一些工业气体的排放)、臭氧层空洞(氟利昂的排放)、温室效应(温室气体的排放,二氧化碳,甲烷等)等环境问题的原因进行分析判断即可.
解答 解:
A、超音速飞机尾气含有二氧化硫、氮氧化物等有害气体,故不符合题意;
B、使用太阳能淋浴器是利用太阳光的辐射能量,不会产生二氧化碳、二氧化硫、氟利昂等有害气体.故符合题意;
C、燃烧煤可产生二氧化碳等有害气体,故不符合题意;
D、使用氟利昂作制冷剂可导致臭氧层空洞.故不符合题意.
故选:B.
点评 本题难度不大,了解酸雨、臭氧层空洞、温室效应等环境问题形成的原因即可正确解答本题.

练习册系列答案
相关题目
13.向盛有10ml稀硫酸的烧杯中加入氢氧化钾溶液,用pH试纸测定烧杯中溶液的pH,所得数据如下表.
请回答下列问题:
(1)写出反应的化学方程式H2SO4+2KOH═K2SO4+2H2O.
(2)当加入氢氧化钾溶液的体积为10ml时,硫酸和氢氧化钾溶液恰好完全反应.
(3)当加入氢氧化钾溶液的体积为15ml时,向溶液中滴入几滴石蕊试液,溶液显蓝色.
(4)当烧杯中溶液的pH=3时,溶液中的溶质是K2SO4、H2SO4.
| 加入氢氧化钾溶液的体积/ml | 0 | 5 | 10 | 15 | 20 |
| 烧杯中溶液的pH | 2 | 3 | 7 | 11 | 12 |
(1)写出反应的化学方程式H2SO4+2KOH═K2SO4+2H2O.
(2)当加入氢氧化钾溶液的体积为10ml时,硫酸和氢氧化钾溶液恰好完全反应.
(3)当加入氢氧化钾溶液的体积为15ml时,向溶液中滴入几滴石蕊试液,溶液显蓝色.
(4)当烧杯中溶液的pH=3时,溶液中的溶质是K2SO4、H2SO4.
14.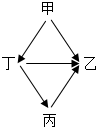 甲、乙、丙、丁四种金属相互转化关系如下图所示,其中金属活动性最弱的是( )
甲、乙、丙、丁四种金属相互转化关系如下图所示,其中金属活动性最弱的是( )
 甲、乙、丙、丁四种金属相互转化关系如下图所示,其中金属活动性最弱的是( )
甲、乙、丙、丁四种金属相互转化关系如下图所示,其中金属活动性最弱的是( )| A. | 甲 | B. | 乙 | C. | 丙 | D. | 丁 |
12.核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
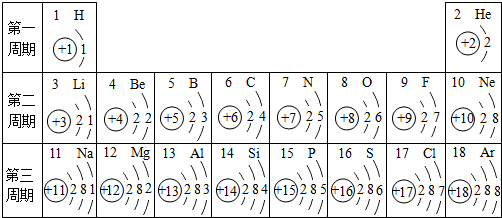
(1)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,各原子核外电子排布的变化规律是最外层电子数依次增加.
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子Na+,阴离子F-.
(4)写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个:
(5)在金属活动性顺序中镁的活动性比铝的活动性强,试从原子结构的角度说明其原因:镁铝的电子层数相同,镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子.

(1)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,各原子核外电子排布的变化规律是最外层电子数依次增加.
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子Na+,阴离子F-.
(4)写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个:
| 物质的类别 | 氧化物 | 酸 | 碱 | 盐 |
| 物质的化学式 |
13.下列物质属于化合物的是( )
| A. | 镁 | B. | 氧气 | C. | 蒸馏水 | D. | 金刚石 |
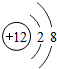 (2)三个水分子3H2O
(2)三个水分子3H2O 框图中B用于改良酸性土壤,J是最常见的金属,G是红棕色物质,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝,在溶液D中滴入AgNO3溶液产生难溶于硝酸的白色沉淀.
框图中B用于改良酸性土壤,J是最常见的金属,G是红棕色物质,E、F、I为无色气体,I能使湿润的红色石蕊试纸变蓝,在溶液D中滴入AgNO3溶液产生难溶于硝酸的白色沉淀.