题目内容
8.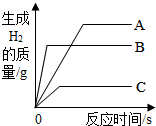 将质量相等的A、B、C三种金属(均为+2价),同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )
将质量相等的A、B、C三种金属(均为+2价),同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )| A. | 放出H2的质量是A>B>C | B. | 金属活动性顺序是A>B>C | ||
| C. | 反应速率最大的是A | D. | 相对原子质量是C<B<A |
分析 根据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断三种金属活动性;
根据一定质量的质量完全反应产生氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,结合三种金属的化合价及完全反应放出氢气的质量大小,判断三种金属的相对原子质量的大小.
解答 解:A、根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是A>B>C;故A正确;
B、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内B放出氢气的质量大于A、大于C,可判断三种金属中B的活动性最强;故B不正确;
C、根据反应生成H2的质量与反应时间的关系图所示,等质量的三种金属B最先完全反应,因此反应速度最大的是B而不是A;故C不正确;
D、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是A>B>C;因此可判断相对原子质量是C>B>A;故D不正确;
故选A.
点评 对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比.

练习册系列答案
相关题目
19.在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后个物质的质量如表所示.根据表中信息判断下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 2 | 30 | 20 | 10 |
| 反应后的质量/g | m | 39 | 5 | 16 |
| A. | 该反应是化合反应 | |
| B. | 甲是该反应的催化剂 | |
| C. | 反应过程中乙、丙变化的质量比为3:5 | |
| D. | 丙可能是单质 |
20.原子论是下列哪位科学家提出的( )
| A. | 道尔顿 | B. | 阿伏加德罗 | C. | 瑞利 | D. | 拉瓦锡 |
17.PM2.5是造成雾霾天气“元凶”之一,下列做法不会增加空气中的PM2.5的是( )
| A. | 工厂排放烟尘 | B. | 外出时佩戴防雾霾口罩 | ||
| C. | 燃放鞭炮 | D. | 焚烧秸秆 |
18.通过化学学习,我们了解了生活中物质变化的本质.下列变化中与其它不同的是( )
| A. | 木柴劈成块 | B. | 西瓜榨成汁 | C. | 海水晒盐 | D. | 米饭变馊 |