题目内容
 现有一包只含有氯化钙杂质的粗盐样品.某校化学兴趣小组的同学为测定该粗盐样品中氯化钙的质量分数,称取该粗盐样品10g,充分溶解于72g水中,再滴加适量的碳酸钠溶液,产生沉淀的质量与加入碳酸钠溶液的质量关系如图所示.试计算:
现有一包只含有氯化钙杂质的粗盐样品.某校化学兴趣小组的同学为测定该粗盐样品中氯化钙的质量分数,称取该粗盐样品10g,充分溶解于72g水中,再滴加适量的碳酸钠溶液,产生沉淀的质量与加入碳酸钠溶液的质量关系如图所示.试计算:(1)该粗盐样品中氯化钙的质量分数.(精确到0.1%)
(2)过滤后所得滤液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据沉淀碳酸钙的质量可以计算氯化钙的质量以及反应生成氯化钠的质量;
根据氯化钙的质量可以计算样品中氯化钠的质量,进一步可以计算该粗盐样品中氯化钙的质量分数以及过滤后所得滤液中溶质的质量分数.
根据氯化钙的质量可以计算样品中氯化钠的质量,进一步可以计算该粗盐样品中氯化钙的质量分数以及过滤后所得滤液中溶质的质量分数.
解答:解:(1)设粗盐样品中氯化钙的质量为x,生成的NaCl质量为y,
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100 117
x 2.0g y
=
=
,
x=2.22g,y=2.34g,
该粗盐样品中氯化钙的质量分数为:
×100%=22.2%,
答:该粗盐样品中氯化钙的质量分数为:
×100%=22.2%.
(2)该粗盐样品中氯化钠的质量为:10g-2.22g=7.78g,
过滤后所得滤液中溶质的质量分数为:
×100%=10%,
答:过滤后所得滤液中溶质的质量分数为10%.
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100 117
x 2.0g y
| 111 |
| x |
| 100 |
| 2.0g |
| 117 |
| y |
x=2.22g,y=2.34g,
该粗盐样品中氯化钙的质量分数为:
| 2.22g |
| 10g |
答:该粗盐样品中氯化钙的质量分数为:
| 2.22g |
| 10g |
(2)该粗盐样品中氯化钠的质量为:10g-2.22g=7.78g,
过滤后所得滤液中溶质的质量分数为:
| 7.78g+2.34g |
| 10g+72g+21.2g-2.0g |
答:过滤后所得滤液中溶质的质量分数为10%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
“抓好资源节约,建设环境友好型社会”是我国社会和经济长期发展的重要保证.你认为下列做法与之不相符的是( )
| A、合理和综合利用煤和石油 |
| B、大量使用农药和化肥提高粮食产量 |
| C、及时关闭水龙头 |
| D、积极开发和利用太阳能、风能和地热能等能源 |
把少量的下列物质分别放入水中,振荡后能形成溶液的是( )
| A、胡椒粉 | B、蔗糖 |
| C、花生油 | D、面粉 |
下列各组物质按照单质、氧化物、混合物的顺序排列的是( )
| A、氮气 氧气 空气 |
| B、水银 水 糖水 |
| C、金刚石 石墨 C60 |
| D、生石灰 熟石灰 石灰石 |
下列实验操作错误的是( )
A、 加入固体粉末 |
B、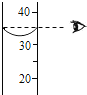 读取液体体积 |
C、 加热液体物质 |
D、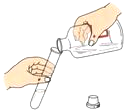 倾倒液体物质 |