题目内容
16.下列实验所对应的两种方案均正确的是( )| 选项 | 目的 | 方案- | 方案二 |
| A | 除去木炭粉中的氧化铜 | 加足量盐酸,过滤 | 在空气中充分燃烧 |
| B | 分离NaCl和CaCO3的混合物 | 溶解、过滤、蒸发滤液 | 加足量稀盐酸,蒸发 |
| C | 检验稀盐酸和稀NaOH溶液 | 分别测溶液的pH | 取样,加CuSO4溶液 |
| D | 鉴别蒸馏水和食盐水 | 取样,加热蒸发 | 取样,加肥皂水 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
B、根据氯化钠易溶于水,碳酸钙难溶于水;碳酸钙能与稀盐酸反应生成氯化钙,进行分析判断.
C、根据稀盐酸和稀NaOH溶液分别显酸性、碱性,氢氧化钠溶液能与硫酸铜溶液反应生成氢氧化铜蓝色沉淀,进行分析判断.
D、根据蒸发食盐水会得到白色固体,蒸馏水和食盐水均不含可溶性钙镁化合物,进行分析判断.
解答 解:A、氧化铜能与稀盐酸反应生成氯化铜和水,木炭不能与稀盐酸反应,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则;木炭粉在空气中充分燃烧生成二氧化碳气体,反而会把原物质除去,不符合除杂原则;故选项实验所对应的两种方案有一种有错误.
B、氯化钠易溶于水,碳酸钙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离;CaCO3能与稀盐酸反应生成氯化钙、水和二氧化碳,再蒸发,得到的是氯化钠和氯化钙的混合物;故选项实验所对应的两种方案有一种有错误.
C、稀盐酸和稀NaOH溶液分别显酸性、碱性,分别测溶液的pH,小于7的是稀盐酸,大于7的是氢氧化钠溶液;氢氧化钠溶液能与硫酸铜溶液反应生成氢氧化铜蓝色沉淀,取样,加CuSO4溶液,沉淀蓝色沉淀的是氢氧化钠溶液,无明显变化的是稀盐酸;故选项实验所对应的两种方案均正确.
D、蒸馏水和食盐水,得到白色固体的是食盐水;蒸馏水和食盐水均不含可溶性钙镁化合物,取样,加肥皂水,均产生大量的泡沫,不能鉴别;故选项实验所对应的两种方案有一种有错误.
故选:C.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
4.推理是一种重要的学习方法.下列推理中正确的是( )
| A. | 酸和碱发生中和反应生成盐和水,则生成盐和水的化学反应一定是中和反应 | |
| B. | 酸性溶液能使紫色石蕊溶液变红,则能使紫色石蕊溶液变红的一定是酸性溶液 | |
| C. | 饱和溶液不能继续溶解某种溶质.则其它物质也不能继续溶解在该饱和溶液中 | |
| D. | 同种分子构成的物质一定是纯静物,则纯净物一定都是由同种分子构成的 |
11.下列各种物质中,同种元素的化合价均相同的是( )
| A. | HCl KClO3 | B. | K2MnO4 KMnO4 | ||
| C. | NH3 HNO3 | D. | NaHCO3 Na2CO3 |
1.下列化学符号书写正确的是( )
| A. | 2个氮分子:2N | B. | 2个氢氧根离子:2(OH)- | ||
| C. | 硝酸铁:Fe(NO)3 | D. | 碳酸钙中碳元素的化合价:Ca$\stackrel{+4}{C}$O3 |
8.小刚在家中准备丢弃的红枣袋中发现一袋双吸剂,其标签如图1所示.拿到学校后同学们对这包久置的固体样品也很好奇,于是在老师的指导下进行了如下探究:
【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】小刚设计了方案一:
同学们认为小刚的方案一并不能得出一定不含Fe2O3的结论,理由是:氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也
是浅绿色.大家讨论后设计如图2实验二方案继续验证.
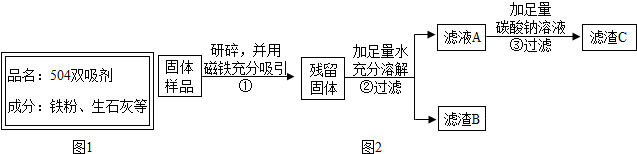
步骤②中固体溶解时放出热量,由此可以判断固体中一定含有CaO.
写出该过程中反应的化学方程式CaO+H2O=Ca(OH)2.
同学们对滤渣B再进行探究:
【实验结论】该久置固体中一定含有Fe、Fe2O3、CaO、CaCO3.
【反思】食品包装袋内放双吸剂的目的是吸收食品包装袋内的氧气和水分,防止食品腐败.
【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】小刚设计了方案一:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管 中,滴加足量的稀盐酸. | 固体逐渐消失,有无色气泡产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3. |
是浅绿色.大家讨论后设计如图2实验二方案继续验证.

步骤②中固体溶解时放出热量,由此可以判断固体中一定含有CaO.
写出该过程中反应的化学方程式CaO+H2O=Ca(OH)2.
同学们对滤渣B再进行探究:
| 实验操作 | 实验现象 | 实验结论 |
| 取滤渣B于试管中,加入适量稀盐酸,生成的气体通入澄清石灰水 | 固体减少,产生气泡,溶液变为黄色 石灰水变浑浊. | 固体中一定含有CaCO3和Fe2O3. |
【反思】食品包装袋内放双吸剂的目的是吸收食品包装袋内的氧气和水分,防止食品腐败.
5.锰丝放入稀硫酸中,有气泡产生,放入硫酸铝溶液中,表面没有金属析出.下列关于锰活动性判断不正确的是( )
| A. | Mn>Cu | B. | Al>Mn | C. | Mn>H | D. | Mn>Mg |
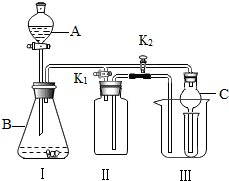 某校化学兴趣小组设计的实验装置如图所示,既可用于制取气体,又可用于验证物质性质.
某校化学兴趣小组设计的实验装置如图所示,既可用于制取气体,又可用于验证物质性质.